Содержание:
Что такое кожная токсичность?
Кожная токсичность – это кожные реакции, которые появляются более чем у 80% пациентов на фоне системной лекарственной противоопухолевой терапии. Эти реакции являются результатом токсического, угнетающего воздействия химиотерапии на растущие, быстроделящиеся клетки организма, в том числе клетки кожи, волос и ногтей. Так ранние реакции развиваются через 1-2 недели, отсроченные реакции через 3-5 недель и поздние реакции через 6 и более недель.
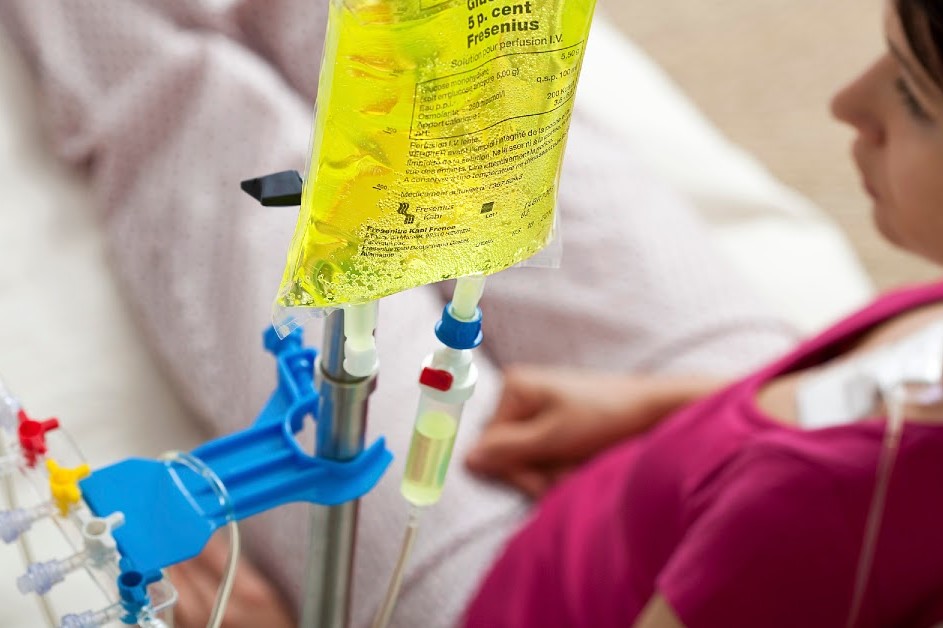
При химиотерапии кожа у пациента становится очень сухой, истончается, шелушится, трескается; может появляться кожный зуд. На лице, голове, туловище появляются акнеподобные (угревые) высыпания. На ладонях и подошвах кожа краснеет, грубеет, трескается, шелушится. На туловище и конечностях могут появляться высыпания в виде пятен и узелков. При попадании на кожу солнечных лучей могут возникать фотоаллергические реакции. Развивается выпадение волос, изменения ногтей и ногтевых валиков.
Типы кожной токсичности
К настоящему моменту описано более 30 различных вариантов кожной токсичности. Наиболее часто встречаются:
- акнеподобные (угревые) высыпания;
- ксероз (сухость, истончение, шелушение) кожи;
- кожный зуд;
- ладонно-подошвенная кожная реакция;
- ладонно-подошвенный синдром;
- пятнисто-папулезные высыпания (в виде пятен и узелков);
- фотореакции (патологические кожные реакции на солнце);
- изменения роста волос и ногтей;
- новообразования кожи и другие.
Химиотерапия, таргетная терапия и кожная токсичность
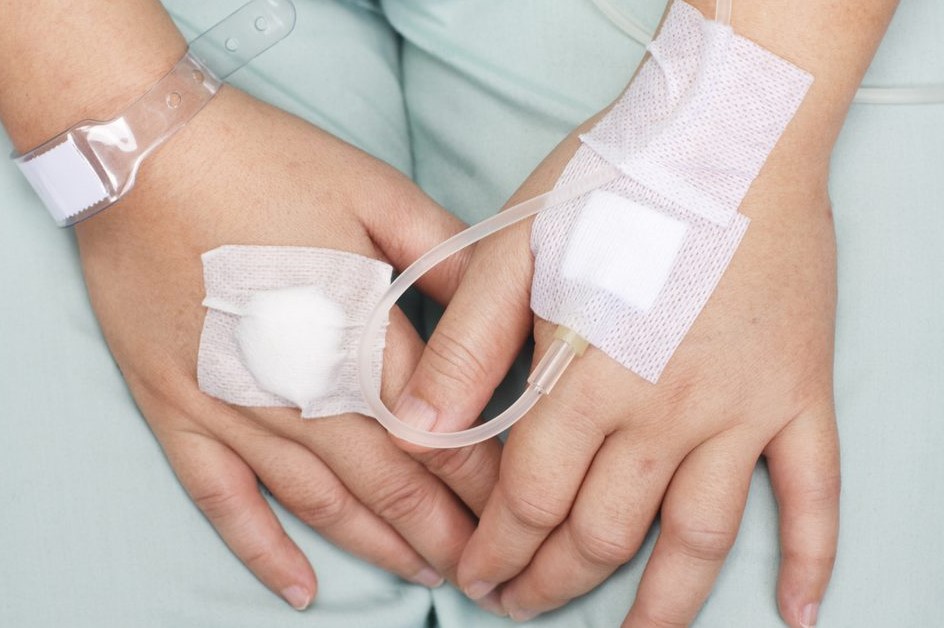
Для различных видов противоопухолевой терапии характерны свои особенности кожных реакций.
Так при химиотерапии (цитостатики) нарушаются процессы роста и механизмы деления всех клеток организма, а не только опухолевых. При этом происходит прямое цитотоксическое действие на клетки кожи и ее придатков, вследствие чего развиваются ладонно-подошвенный синдром, нарушение пигментации кожи, выпадение волос, изменение ногтей.
При таргетной терапии клетки кожи становятся «второй мишенью», помимо опухолевых клеток, так как несут на себе те же рецепторы, блокируемые препаратом. Например, препараты ингибиторы EGFR (эпидермального фактора роста) подавляют рост клеток кожи, волос и ногтей, вызывают выброс повреждающих тканевых ферментов и асептическое воспаление. В результате развиваются акнеподобные (угревые) высыпания, ксероз (сухость, истончение, шелушение) кожи, изменения волос и ногтей, поражение слизистых оболочек, ладонно-подошвенные кожные реакции, фотореакции (патологические кожные реакции на солнце).
Степень кожной токсичности
При оценке степени тяжести кожной токсичности учитывается площадь поражения, объективное ухудшение кожного процесса, выраженность субъективных ощущений пациента, нарушение его повседневной жизнедеятельности.
Так, например, по выраженности угревой (акнеподобной) сыпи выделяют 4 степени процесса:
I степень — площадь высыпаний менее 10%, возможен кожный зуд (болезненность);
II степень — площадь высыпаний 10-30%, кожный зуд (болезненность), негативное психологическое воздействие, ограничение активности;
III степень — площадь высыпаний более 30% кожный зуд (болезненность), негативное психологическое воздействие, ограничение самообслуживания, возможна локальная суперинфекция;
IV степень — площадь высыпаний любая связанная с распространенной суперинфекцией, требующей назначения внутривенной антибиотикотерапии, жизнеугрожающее состояние.
Таким образом, более тяжелые степени кожной токсичности требуют более активной терапии, снижения дозы химиопрепаратов, а при тяжелой III-IV степени приходится прерывать противоопухолевую терапию.
Первая помощь при кожной токсичности

Уже накануне противоопухолевой терапии врач-онколог назначает профилактическую терапию кожной токсичности, которая включает в себя:
- нанесение аптечных увлажняющих кремов-эмолентов утром;
- нанесение глюкокортикоидных кремов вечером (с активностью не выше 1% гидрокортизоновой мази);
- нанесение аптечных солнцезащитных кремов на открытые участки тела перед выходом на улицу в период с весны по осень (с фильтрами SPF>20, PPD>1/3 SPF)
- при таргетной терапии дополнительно назначаются антибиотики тетрациклинового ряда в противовоспалительной дозировке.
Если на фоне профилактической терапии проявления кожной токсичности все-таки прогрессируют, необходимо сообщить об этом лечащему врачу и получить консультацию врача-дерматолога (дерматовенеролога), который назначит дополнительное лечение кожной токсичности.
Кроме того, пациенты с наличием хронических кожных заболеваний должны получить консультацию врача-дерматолога еще перед началом курса химиотерапии.
Чем опасно отсутствие лечения кожной токсичности?
При отсутствии лечения кожной токсичности возможно развитие распространенной суперинфекции, тяжелого жизнеугрожающего состояния и прерывание курса системной лекарственной противоопухолевой терапии.
Как правильно ухаживать за кожей во время химиотерапии?

Полностью избежать кожной токсичности невозможно, но при помощи следующих профилактических мероприятий можно уменьшить ее интенсивность:
- использование мягких синдетных моющих средств, мягких полотенец;
- увлажнение кожи, кремы-эмоленты 2 раза в день;
- аптечные солнцезащитные кремы с максимальными фильтрами;
- исключение макияжа, травм, агрессивных процедур (обрезной маникюр, электробритвы и др.)
- рекомендован аппаратный медицинский педикюр в подологическом кабинете;
- ограничить физические нагрузки на стопы и пальцы кистей;
- ношение головных уборов, просторной мягкой хлопчатобумажной одежды;
- ношение просторной и удобной обуви с ортопедическими стельками;
- пользоваться хлопчатобумажными защитными перчатками;
- избегать воздействия бытовой химии, раздражителей и спиртовых растворов;
- ограничить водные процедуры (горячий душ, ванны, баня);
- в рационе питания должны быть продукты богатые кальцием, железом, цинком, витаминами А, Е и омега 3-6-9 жирными кислотами;
- при наличии заболеваний кожи, ногтей и волос, либо если такие проблемы были ранее, необходимо получить консультацию врача-дерматолога (дерматовенеролога)
Что делать, если возникает зуд?
Если пациент получает профилактическую терапию кожной токсичности: увлажняющие кремы-эмоленты утром, 1% гидрокортизоновый крем вечером, солнцезащитный крем и все-таки возникает зуд, — следует обратиться к лечащему врачу, либо на консультацию врача-дерматолога (дерматовенеролога).
Для облегчения зуда можно дополнительно нанести на зудящие области кремы-эмоленты. Внутрь можно принять 1 таблетку антигистаминного препарата 2-го поколения.
Что делать, если возникает сыпь?
Если пациент применяет профилактическую терапию кожной токсичности и при этом развивается сыпь, следует обратиться к лечащему врачу, который оценит степень тяжести, назначит дополнительное лечение, либо консультацию врача-дерматолога (дерматовенеролога).
Что делать, если поднялась температура?
Следует сообщить об этом лечащему врачу. При повышении температуры тела выше 38 гр. необходимо принять внутрь нестероидный противовоспалительный препарат.
Что делать, если есть сухость и шелушения?
Сухость и шелушение хорошо корректируются при помощи кремов-эмолентов, которые можно наносить 2 и более раз в сутки.
Что делать, если кожа меняет цвет?
Гиперпигментация кожи обычно развивается через 2–3 недели после окончания химиотерапии или на 10–12 неделе после начала курса лечения. Появляются окрашенные пятна на кончиках пальцев, локтевых суставах или ладонях, лице, вдоль используемых для инъекции вен.
Гиперпигментация дополнительного лечения не требует. После окончания курса противоопухолевой терапии она постепенно исчезнет. Специфической профилактики нет.
Как вести себя на солнце во время проведения курса химиотерапии?
Необходимо исключить пребывание на солнце. Рекомендовано ношение одежды с длинным рукавом, головной убор с широкими полями, солнцезащитные очки. Для верхней одежды предпочтение следует отдавать льняным тканям как более эффективным в отношении солнцезащиты, чем хлопчатобумажные. При этом окрашенные ткани обладают большим защитным эффектом по сравнению с белыми. Кроме того, нейлон, шерсть и полиэстер лучше защищают от ультрафиолетового облучения, чем хлопок.
Даже в холодные периоды года и при отсутствии солнца за 20 мин до выхода на улицу рекомендуется наносить на открытые участки кожи (лицо, кисти и др.) аптечные солнцезащитные кремы с максимальной комплексной защитой: SPF 50+/PPD 46.
Что при кожной токсичности категорически нельзя делать?
Нельзя заниматься самолечением кожной токсичности, в том числе народными средствами и самостоятельно снижать дозу, либо отменять противоопухолевые препараты.
Список литературы:
- Каспаров Б. С., Рогачев М. В., Беляев А. М. и соавт. Амбулаторная онкология. Практические аспекты (Часть 2). Учебное пособие. — Санкт-Петербург: «Грейт Принт», 2020. – 161 с.
- Жуков Н. В. Практическое пособие по сопроводительной терапии в онкологии.— М.: Литтерра, 2008.— 44 с.
- Практические рекомендации Российского общества клинической онкологии.— 2018 г. [Electronic resource]. URL: https://rosoncoweb.ru/standarts/RUSSCO/2019/ (accessed: 20.07.2019)
- Проценко С. А., Антимоник Н. Ю., Берштейн Л. М., Новик А. В. и др. Практические рекомендации по коррекции иммуноопосредованных нежелательных явлений // Злокачественные опухоли: Практические рекомендации RUSSCO.— 2017.— Т. 7, №3.— С. 592-620 5. Проценко С. А., Антимоник Н. Ю., Берштейн Л. М., Новик А. В., Носов Д. А., Петенко Н. Н. и др. Практические рекомендации по управлению иммуноопосредованными нежелательными явлениями // Злокачественные опухоли: Практические рекомендации RUSSCO.— 2018.— Т. 8, № 3.— С. 636–665.
- Российское общество клинической онкологии. Злокачественные опухоли — 2019.— Vol. 9 — P.655–667, P.678–684.
- Alimonti A. et al. Nail disorders in a woman treated with ixabepilone for metastatic breast cancer // Anticancer Res.— 2005.— Vol. 25, № 5.— P. 3531–3532.
- Alley E., Green R., Schuchter L. Cutaneous toxicities of cancer therapy // Curr. Opin. Oncol.— 2002.— Vol. 14, № 2.— P. 212–216.
- Autier J. et al. Prospective study of the cutaneous adverse effects of sorafenib, a novel multikinase inhibitor // Arch. Dermatol.— 2008.— Vol. 144, № 7.— P. 886–892.
- Balagula Y. et al. Clinical presentation and management of dermatological toxicities of epidermal growth factor receptor inhibitors // Int. J. Dermatol.— 2011.— Vol. 50, №2.— P. 129–146 49. Balagula Y., Rosen S. T., Lacouture M. E. The emergence of supportive oncodermatology: The study of dermatologic adverse events to cancer therapies // J. Am. Acad. Dermatol.— 2011.— Vol. 65, № 3.— P. 624–635.
- Batchelor D. Hair and cancer chemotherapy: consequences and nursing care a literature study // Eur. J. Cancer Care (Engl).— 2001.— Vol. 10, № 3.— P. 147–163.
- Bolognia J. L., Cooper D. L., Glusac E. J. Toxic erythema of chemotherapy: A useful clinical term // J. Am. Acad. Dermatol.— 2008.— Vol. 59, № 3.— P. 524–529.
- Bonamichi-Santos R., Castells M. Diagnoses and Management of Drug Hypersensitivity and Anaphylaxis in Cancer and Chronic Inflammatory Diseases: Reactions to Taxanes and Monoclonal Antibodies // Clin. Rev. Allergy Immunol.— 2016.
- Busam K. J. et al. Cutaneous side-effects in cancer patients treated with the antiepidermal growth factor receptor antibody C225 // Br. J. Dermatol.— 2001.— Vol. 144, № 6.— P. 1169–1176 .
- Chen P., Chen F., Zhou B. Systematic review and meta-analysis of prevalence of dermatological toxicities associated with vemurafenib treatment in patients with melanoma // Clin. Exp. Dermatol.— 2019.— Vol. 44, № 3.— P. 243–251.
- Choi J. N. Chemotherapy-induced iatrogenic injury of skin: new drugs and new concepts // Clin. Dermatol.— 2011.— Vol. 29, № 6.— P. 587–601.
- Chon S. Y. et al. Chemotherapy-induced alopecia // J. Am. Acad. Dermatol.— 2012.— Vol. 67, № 1.— P. 37–47.
- Degen A. et al. The hand-foot-syndrome associated with medical tumor therapy — classification and management // J. Dtsch. Dermatol. Ges.— 2010.— Vol. 8, № 9.— P. 652–661.
- Dueland S. et al. Epidermal growth factor receptor inhibition induces trichomegaly // Acta Oncol.— 2003.— Vol. 42, № 4.— P. 345–346.
- Fischer A. et al. The risk of hand-foot skin reaction to axitinib, a novel VEGF inhibitor: a systematic review of literature and meta-analysis // Invest New Drugs.— 2013.— Vol. 31, № 3.— P. 787–797.
- Hu J. C. et al. Cutaneous side effects of epidermal growth factor receptor inhibitors: clinical presentation, pathogenesis, and management // J. Am. Acad. Dermatol.— 2007.— Vol. 56, № 2.— P. 317–326.
- Gressett S. M., Stanford B. L., Hardwicke F. Management of hand-foot syndrome induced by capecitabine // J. Oncol. Pharm. Pract.— 2006.— Vol. 12, № 3.— P. 131–141 71. Gutzmer R. et al. Management of cutaneous side effects of EGFR inhibitors: recommendations from a German expert panel for the primary treating physician // J. Dtsch. Dermatol. Ges.— 2011.— Vol. 9, № 3.— P. 195–203.
- Kouwenhoven T. A., van de Kerkhof P. C. M., Kamsteeg M. Use of oral antidepressants in patients with chronic pruritus: A systematic review // J. Am. Acad. Dermatol.— 2017.— Vol. 77, № 6.— P. 1068–1073.
- Lacouture M. E. et al. Clinical practice guidelines for the prevention and treatment of EGFR inhibitor-associated dermatologic toxicities // Support Care Cancer.— 2011.— Vol. 19, № 8.— P. 1079–1095.
- Lacouture M. E. et al. Evolving strategies for the management of hand-foot skin reaction associated with the multitargeted kinase inhibitors sorafenib and sunitinib // Oncologist.— 2008.— Vol. 13, № 9.— P. 1001–1011.
- Lee M.-W. et al. Cutaneous side effects in non-small cell lung cancer patients treated with Iressa (ZD1839), an inhibitor of epi-dermal growth factor // Acta Derm. Venereol.— 2004.— Vol. 84, № 1.— P. 23–26.
- Mangili G. et al. Prevention strategies in palmar-plantar erythrodysesthesia onset: the role of regional cooling // Gynecol. On-col.— 2008.— Vol. 108, № 2.— P. 332–335.
- Matsuda K. M. et al. Gabapentin and pregabalin for the treatment of chronic pruritus // J. Am. Acad. Dermatol.— 2016.— Vol. 75, № 3.— P. 619–625.
- Masters J. C., Nickens D. J., Xuan D., Shazer R. L., & Amantea M. Clinical toxicity of antibody drug conjugates: a meta-analysis of payloads // Investigational New Drugs.— 2017.— № 36.— Р. 121–135 100. McGarvey E. L. et al. Psychological sequelae and alopecia among women with cancer // Cancer Pract.— 2001.— Vol. 9, № 6.— P. 283–289.
- McLellan B. et al. Regorafenib-associated hand–foot skin reaction: practical advice on diagnosis, prevention, and management // Ann. Oncol.— 2015.— Vol. 26, № 10.— P. 2017–2026.
Что вам необходимо сделать
Если вы хотите узнать побольше о бесплатных возможностях ФБГУ НМИЦ онкологии им. Н.Н. Петрова Минздрава России, получить очную или заочную консультацию по диагностике и лечению, записаться на приём, ознакомьтесь с информацией на официальном сайте.
Если вы хотите общаться с нами через социальные сети, обратите внимание на аккаунты в ВКонтакте и Одноклассники.
Если вам понравилась статья:
- оставьте комментарий ниже;
- поделитесь в социальных сетях через удобные кнопки:





