Содержание:
Среди онкологических заболеваний рак молочной железы (РМЖ) у женщин занимает 1 место и является одной из самых распространенных причин смертности женщин от онкологических заболеваний.
По данным Всемирной организации здравоохранения (WHO) в 2020 году было зарегистрировано свыше 2,2 миллиона случаев заболевания. Считается, что в течение жизни заболеть раком молочной железы может каждая двенадцатая женщина.
Рак молочной железы возникает в эпителиальных клетках протоков (85 %) или долек (15 %) железистой ткани молочной железы. Сначала рост опухоли ограничивается протоком или долькой (преинвазивный рак, «рак на месте» – in situ, 0 стадия), где он не вызывает никаких симптомов и очень редко метастазирует.
Со временем рак in situ разрастается и переходит в инвазивный рак молочной железы, а затем может распространиться в близлежащие лимфатические узлы (регионарное метастазирование), а потом и в другие органы (отдаленное метастазирование).
Раннее выявление опухоли на доклинической стадии, когда женщину еще ничего не беспокоит, позволяет провести своевременное лечение, которое способно полностью излечить РМЖ. Лечение часто является комбинированным, включающим хирургическую операцию по удалению опухоли, лучевую терапию и лекарственное лечение.
Рак вызывает страх. Он до сих пор остается самым сильным стрессовым фактором. Существует медицинский термин «канцерофобия» или боязнь заболеть раком, но времена изменились – сейчас резко повысились эффективность ранней диагностики и качество лечения.
По статистическим данным, из всех заболеваний молочных желез на долю рака приходится только 10 %. Это означает, что если вы обнаружили образование в своей молочной железе, то оно, скорее всего, доброкачественное, но его обязательно нужно показать врачу. К доброкачественным образованиям относятся кисты, фиброаденомы. Однако существуют некоторые изменения, которые со временем могут перейти в злокачественные. Об этом должен знать ваш врач и вовремя назначить правильное лечение.
Современное лечение также изменилось. Еще 10 лет назад хирургическое лечение заключалось в основном в полном удалении молочной железы – мастэктомии.
Сейчас хирургия направлена на сохранение молочной железы. Все чаще выполняются органосохраняющие операции и реконструкции с помощью имплантов.
Залог успешного и правильного лечения – раннее выявление рака, поэтому важно регулярно проходить обследования.
Что нужно знать пациенту о диагностике молочных желез
Причины, по которым происходит позднее выявление РМЖ, можно разделить на две категории.
Первая заключается в том, что часть женщин, проживающих в районных городах и сельских поселениях, не имеет возможность посещать врача-онколога (маммолога) из-за нехватки медицинских кадров или их отсутствия.
Среди причин необращений можно определить следующие:
- недостаточное количество или отсутствие специалистов и оборудования в медицинских учреждениях;
- низкая информированность о современных методах диагностики и лечения заболеваний молочной железы;
- долгое ожидание записи на маммографию;
- ответственное отношение к здоровью членов семьи и безответственное к собственному;
- страх.
Вторая – женщины обращаются к профильным специалистам с жалобами, проходят большое количество обследований и получают противоречивые диагнозы. Пациентки годами ходят по разным учреждениям, но диагноз им устанавливается уже на поздних стадиях.
Причин этого может быть несколько:
- В нашей стране МГ, УЗИ, МРТ исследования выполняют разные специалисты. Каждый оценивает молочную железу через призму своего метода диагностики и ставит свой диагноз. Все три метода основаны на разных физических явлениях и способны определять разные изменения молочной железы. Поэтому данные методы взаимодополняемы, а не взаимозаменяемы. За рубежом все три метода выполняет один специалист и на основании полученных данных выносит один диагноз, а не три как в российской практике.
- Второй ограничивающий фактор – это высокая маммографическая плотность (ВМП) у женщин после 40 лет, которая встречается в 40–50% случаев. Высокая маммографическая плотность – не только фактор риска развития РМЖ, но и фактор, который резко снижает эффективность МГ. На плотном рентгеновском фоне на МГ могут быть пропущены как доброкачественные, так, к сожалению, и злокачественные образования. У таких пациенток в обязательном порядке вместе с МГ должно выполняться УЗИ молочных желез, а в определенных случаях и МРТ.
- Плохая информированность женщин о возможностях диагностических методов и о том, как узнать свой тип строения молочных желез, как и где проходить обследование.
Доступность информации о методах диагностики – это путь к раннему выявлению и своевременному лечению заболеваний молочной железы и возможность снизить смертность женщин от РМЖ.
Плотная молочная железа
Высокая маммографическая плотность молочной железы (ВМП) является высоким и наследуемым показателем риска развития рака молочной железы. ВМП проявляется выраженным белым фоном эпителиальной и стромальной ткани на маммограмме, за которым могут скрываться различные патологические изменения, в том числе и рак. Эффективность МГ исследования у пациенток с ВМП недопустимо низкая и составляет около 50 %. А жировой тип строения молочных желез выглядит темным, и на его фоне четко определяются любые изменения – эффективность маммографии высокая и достигает 99–100 %.
Плотная ткань молочной железы – довольно распространенное явление: около 43 % женщин скринингового возраста (после 40 лет) имеют неоднородную или чрезвычайно плотную грудь.
Как узнать свой тип строения молочной железы?
У всех женщин репродуктивного возраста молочная железа состоит в основном из железистой ткани. Это норма! Это значит, что у молодых женщин МГ будет заведомо не эффективна.
Поэтому до 40 лет МГ проводится только в редких случаях и по строгим показаниям, например, при подозрении на рак молочной железы. Методом выбора в данном случае является ультразвуковое исследование.
А вот у женщин после 40 лет большое количество железистой ткани уже является не только фактором риска, но и ограничивающим фактором для проведения МГ. Поэтому, когда пациентка в 40 лет первый раз выполняет МГ, врач рентгенолог оценивает ее тип строения молочных желез и указывает его в заключении.
Различают четыре типа строения: А, В, С, D.
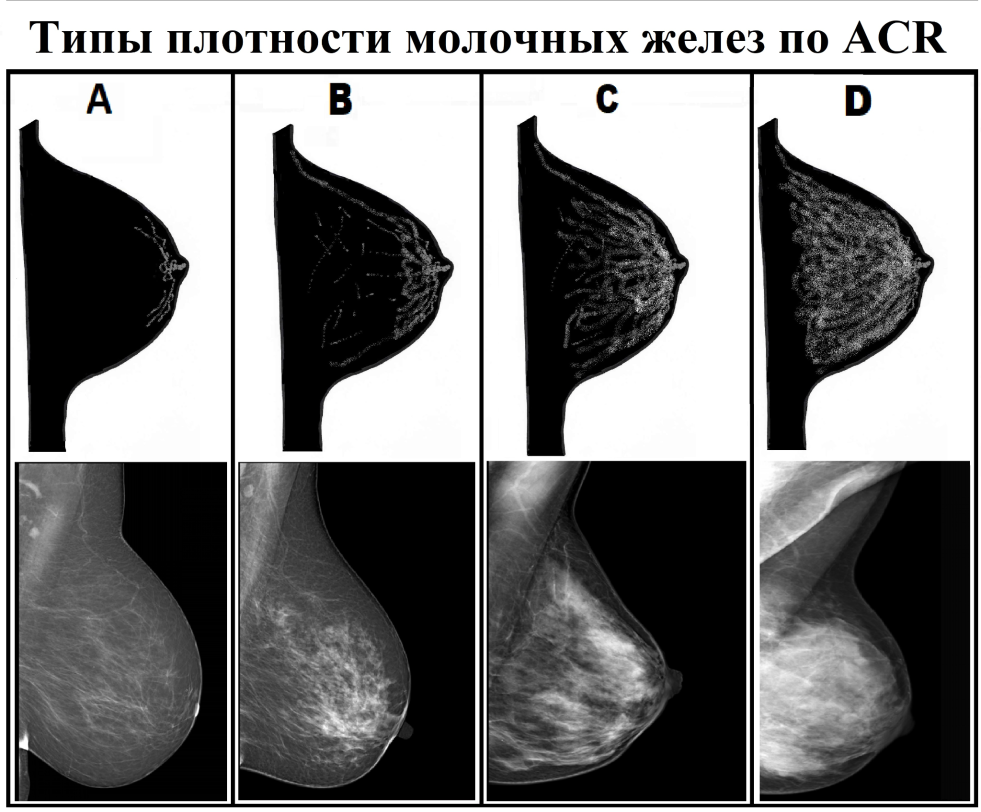
Тип А — жировой тип строения молочных желез.
Тип В — отдельные участки железистой ткани.
Тип С — умеренно выраженная железистая ткань.
Тип D — чрезвычайно выраженная железистая ткань.
Это значит, что пациенткам с типом строения А и В можно дальше наблюдаться при помощи МГ, а вот пациенткам с типом строения C и D необходимо в обязательном порядке помимо МГ выполнять УЗИ.
Что делать если высокая маммографическая плотность молочных желез?
Необходимо знать, что нужно регулярно проходить обследование в профильных медицинских центрах. Пусть вас не пугают названия «Онкологический диспансер» или «Центр онкологии». В этих учреждениях работают специалисты, которые знают особенности наблюдения за такими пациентами.
Маммография
Лучевые методы диагностики развиваются также стремительно, как компьютерные технологии. Появляются новые исследования молочных желез, и пациенткам бывает сложно разобраться, в чем разница. Как правило, новые диагностические методы создаются для того, чтобы обойти главное ограничение классической маммографии – высокую маммографическую плотность.
Что нужно знать о современном маммографическом исследовании?
Маммография (МГ) – это рентгенологическое исследование молочных желез. Любой рентгенологический метод подразумевает лучевую нагрузку или облучение исследуемого органа. Но так ли это страшно? Согласно последним исследованиям, при выполнении цифровой МГ вы получаете такую же лучевую нагрузку как при полете на самолете. Но ценность МГ гораздо выше, ведь вовремя выполненное исследование может спасти жизнь! Тем более что выполнять МГ женщинам после 40 лет рекомендуется раз в два года.
Как выполняется МГ?
Вам сделают четыре снимка: каждую молочную железу рентген-лаборант будет снимать в двух проекциях. Для получения четких изображений требуется выполнить компрессию – сдавление ваших молочных желез.
Помните, что при выполнении МГ недопустимо сдавление, которое вызывает резкую боль и образование гематом!
Какие виды МГ сейчас существуют?
Аналоговая МГ — когда после проведения исследования врач анализирует пленочные изображения. Данный вид маммограммы, если выполнен правильно, решает главную задачу – позволяет определить патологию молочных желез, особенно у женщин с типом строения А и В. Но у данного вида МГ отсутствует возможность редактирования или так называемой цифровой обработки изображений, что возможно только с цифровой МГ.
Цифровая МГ позволяет врачу увеличивать изображение, менять контрастность и яркость, что, несомненно, помогает увидеть больше изменений на снимках. Также цифровые изображения можно архивировать, пересылать между учреждениями, городами и даже странами, а также копировать на диск. Своих пациенток я прошу приносить маммограммы, записанные на диске, так гораздо удобнее работать, и у меня есть возможность получить больше информации, чем если на консультацию принесут пленки.
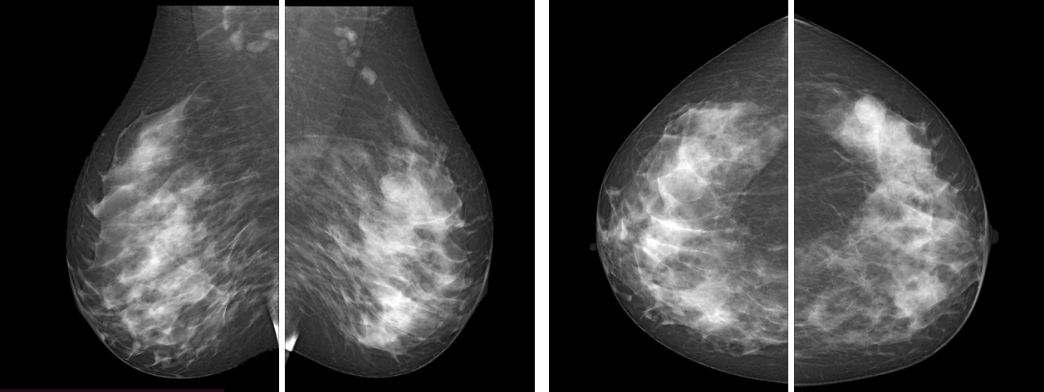
Рис.1 Маммография, выполненная в двух проекциях: фиброаденома левой молочной железы
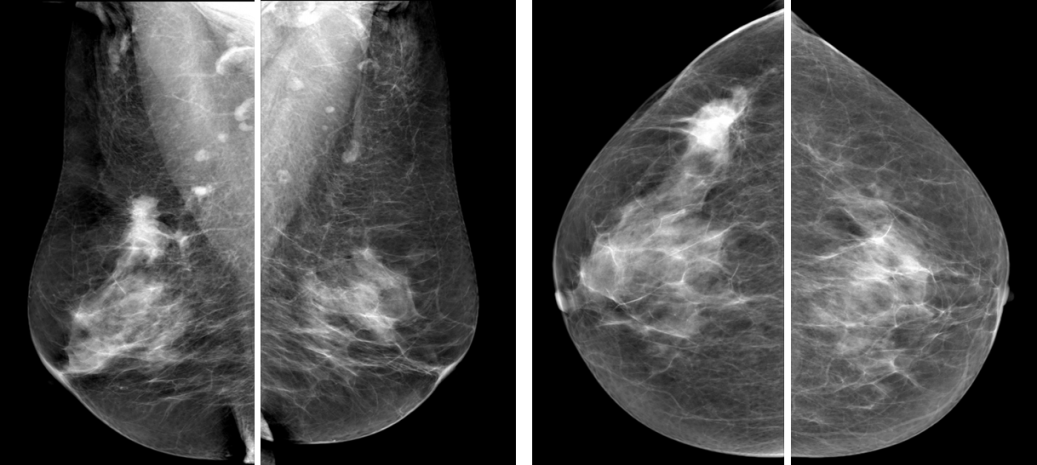
Рис.2 Маммография, выполненная в двух проекциях: рак правой молочной железы
Томосинтез – аналог компьютерной томографии. Это послойное изображение молочных желез. Конечно, лучевая нагрузка при этом возрастет, но незначительно. Также увеличивается польза от этого исследования, ведь у врача появляется возможность послойно, толщиной в 1 мм, изучить весь объем молочных желез. Высокая маммографическая плотность для томосинтеза уже не является таким препятствием, как для аналоговой или цифровой маммографии.
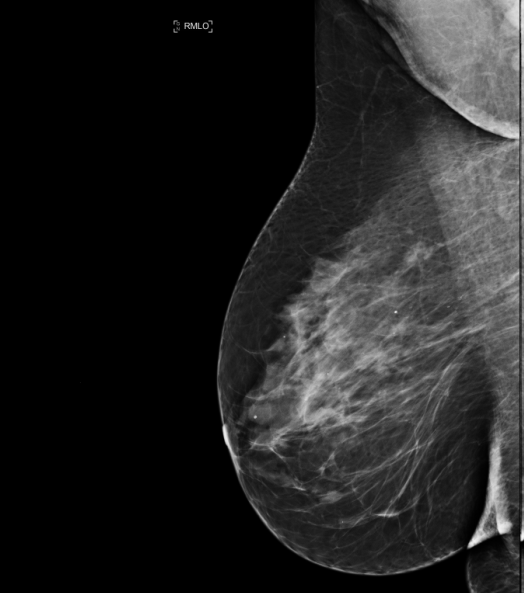
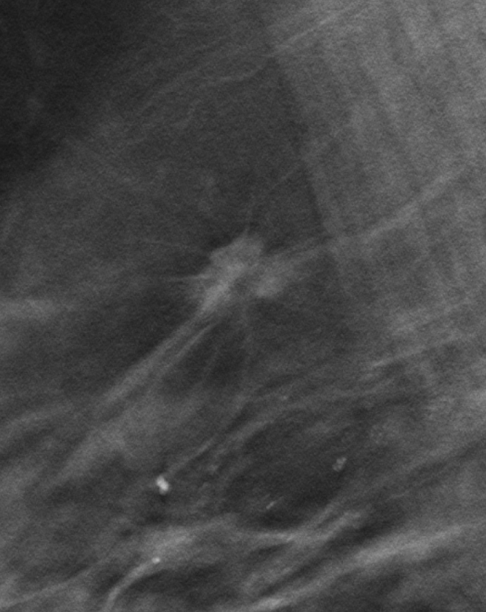
Контрастная спектральная маммография (КСМГ) – инновационный метод диагностики. При выполнении КСМГ вам введут контрастное вещество на основе йода – это позволит врачу увидеть патологические изменения, которые его накапливают. Возможности выявления рака молочной железы у КСМГ выше, чем у других видов МГ.
Но следует помнить, что на йодсодержащие контрастные вещества может быть аллергическая реакция, также они противопоказаны пациентам с патологией почек и печени.
КСМГ может в определенных случаях быть альтернативой МРТ, например, при невозможности выполнить МРТ молочных желез.
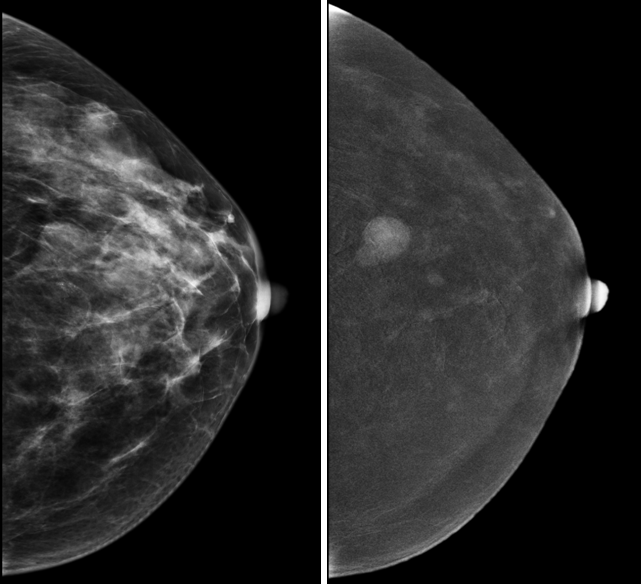
Рис.4 Маммограмма с контрастом: фиброаденома молочной железы
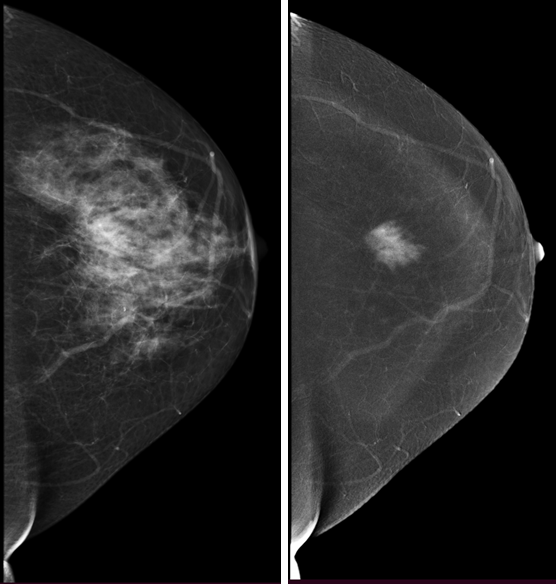
Рис.5 Маммограмма с контрастом: рак молочной железы
Какой рентгенологический метод исследования молочных желез вам подходит?
Конечно, это решает врач, но вы вправе задать ему вопросы относительно своего здоровья. Теперь, понимая разницу и нюансы выполнения видов МГ, вы можете вместе со своим врачом подобрать оптимальный и индивидуальный план обследования, учитывая возможности медицинских учреждений своего региона.
Ультразвуковое исследование молочных желез
УЗИ также относится к бурно развивающимся диагностическим технологиям. Преимуществ у современного, выполненного на экспертном оборудовании УЗИ, достаточно много.
Во-первых, отсутствие лучевой нагрузки – УЗИ можно выполнять молодым, на фоне лактации и даже беременным женщинам.
УЗИ можно выполнять достаточно часто – хоть каждый месяц.
Во-вторых, УЗИ позволяет выявить даже минимальные узловые образования (от 3–4 мм) у пациенток с высокой маммографической плотностью. Именно поэтому у женщин с типом строения C и D по МГ рекомендуется в обязательном порядке выполнять УЗИ.
Сочетание двух методов диагностики молочных желез – МГ и УЗИ – сегодня является самым эффективным диагностическим алгоритмом.
В-третьих, УЗИ является широкодоступным методом, и его можно пройти в любом регионе нашей страны. Однако, как правило, пациентки сталкиваются с неожиданным препятствием – операторозависимостью, ведь качество УЗИ напрямую зависит от квалификации врача и его знаний именно в области диагностики молочной железы. Проконсультировать УЗИ снимки у другого специалиста невозможно, каждый раз нужно повторять исследование. Сегодня набирает популярность мультимодальный подход. Это значит, что вероятность раннего выявления рака молочной железы резко возрастает, когда МГ и УЗИ выполняет и интерпретирует один врач-эксперт.
Как выполняется современное УЗИ молочных желез?
Молодым пациенткам без подозрения на онкологическое заболевание рекомендуется выполнять УЗИ на 6–12 день менструального цикла. Однако если речь заходит о подозрительном образовании, особенно выявленном на МГ, УЗИ можно и нужно выполнять в любой день цикла, так как промедление опасно, а опытный врач УЗИ сможет интерпретировать изображения в любой ситуации. При исследовании вам на кожу нанесут ультразвуковой гель, это необходимо, чтобы ультразвуковые волны свободно проходили в ткань железы.
Помните, что УЗИ молочных желез выполняется без сильной компрессии, болезненности быть не должно.
Какие УЗ-технологии используются в диагностике молочных желез?
Серошкальный В-режим, с помощью которого врач видит строение вашей молочной железы и может выявить патологические изменения, оценить форму, контур и структуру образования.
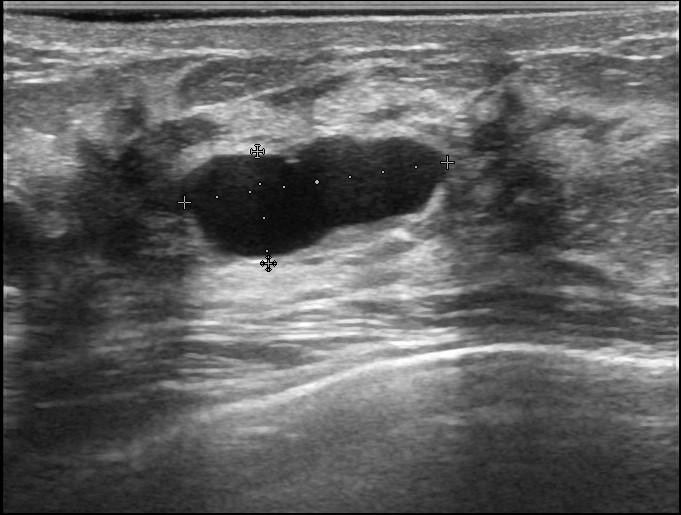
Рис.6 Эхограмма кисты молочной железы
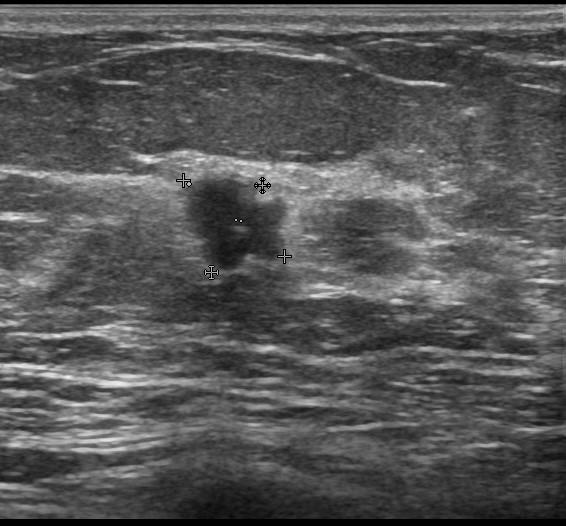
Рис.7 Эхограмма участка аденоза молочной железы
Допплеровский режим определяет кровоток. Важная технология, которая позволяет врачу увидеть сосудистую сеть патологического образования без введения контрастного вещества. Конечно, Допплер не такой чувствительный режим, как контрастирование, но в большинстве случаев он дает важную информацию и способствует раннему выявлению рака.
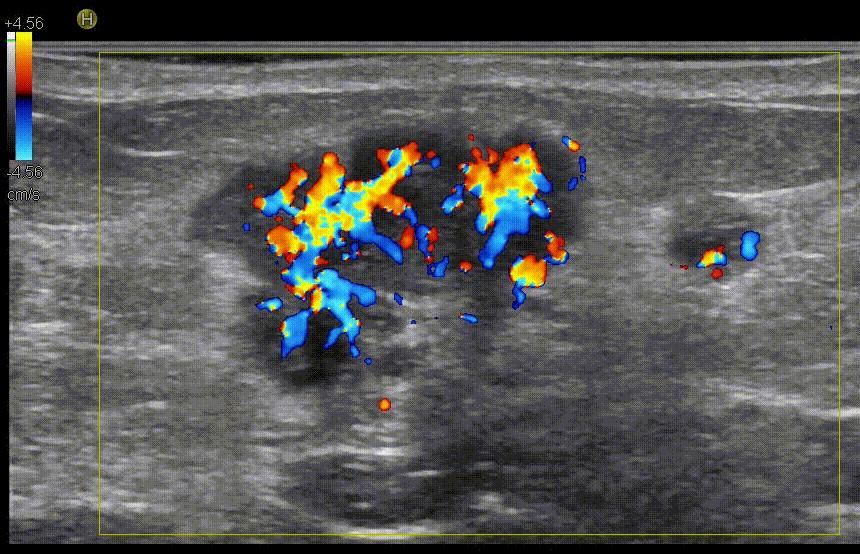
Рис.8 Эхограмма гиперваскулярного рака молочной железы
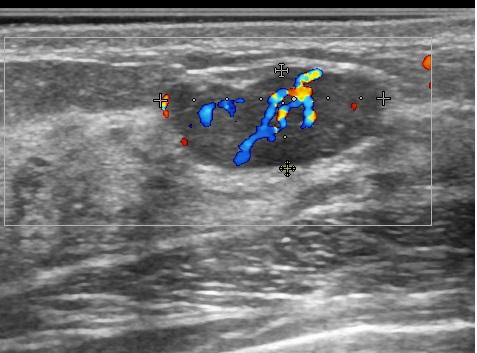
Рис.9 Эхограмма гиперваскулярной фиброаденомы молочной железы
Эластография – инновационная ультразвуковая технология, ее еще называют ультразвуковой пальпацией. Известно, что рак молочной железы имеет более жесткую структуру, чем доброкачественные изменения. Именно эту характеристику и определяет эластография – она измеряет жесткость. Когда врач проводит вам эластографическое исследование – жесткие, а значит подозрительные образования, окрашиваются синим цветом, а эластичные (доброкачественные) – зеленым и желтым. Эластография порой имеет решающее значение.
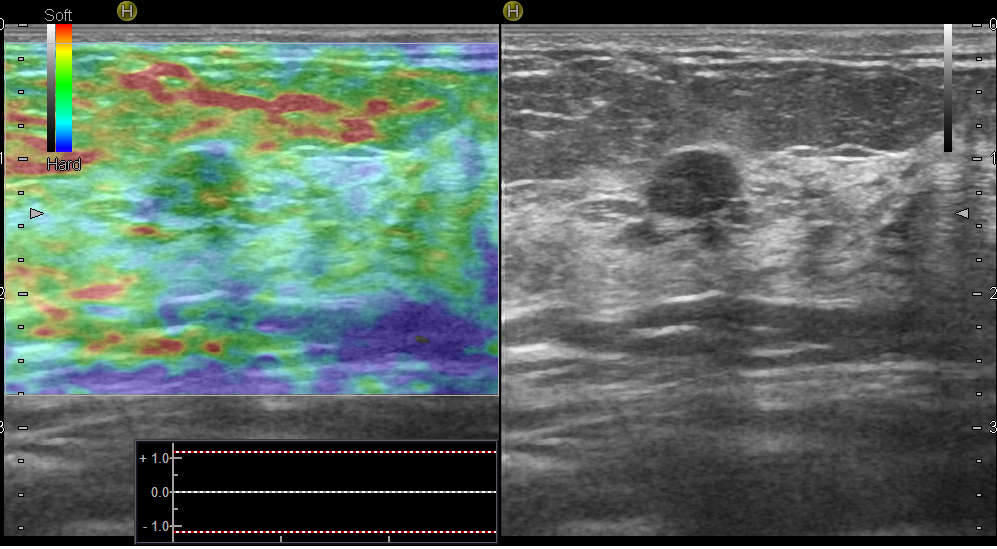
Рис.10 Эластограмма эластичного образования – фиброаденомы молочной железы
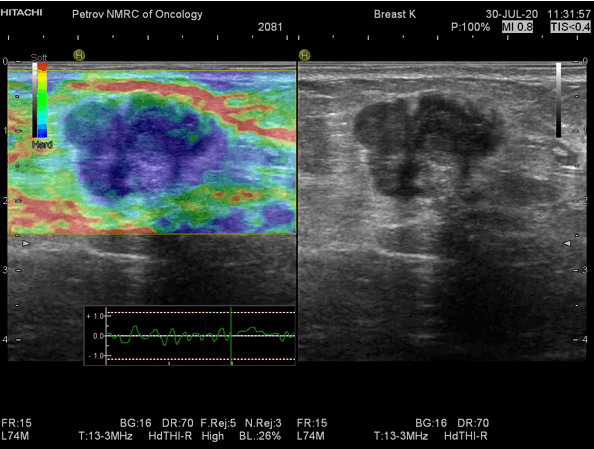
Рис.11 Эластограмма жесткого образования – рака молочной железы
Контрастно-усиленное ультразвуковое исследование –эффективный, но крайне редко используемый метод, в принципе, как и контрастная спектральная маммография. При УЗИ используется контрастное вещество, которое на сегодняшний день считается самым безопасным, то есть практически не вызывающим аллергическую реакцию. Ультразвуковой контраст – это микропузырьки инертного газа гексафторида серы. Через 15–20 минут после исследования пациент полностью выдыхает их через легкие.
Противопоказанием для использования ультразвукового контраста является тяжелая патология сердечной и легочной системы.
Также при контрастном УЗИ отсутствует лучевая нагрузка. Контрастирование позволяет достоверно оценить сосудистую сеть образования, что резко повышает эффективность раннего выявления рака молочной железы.
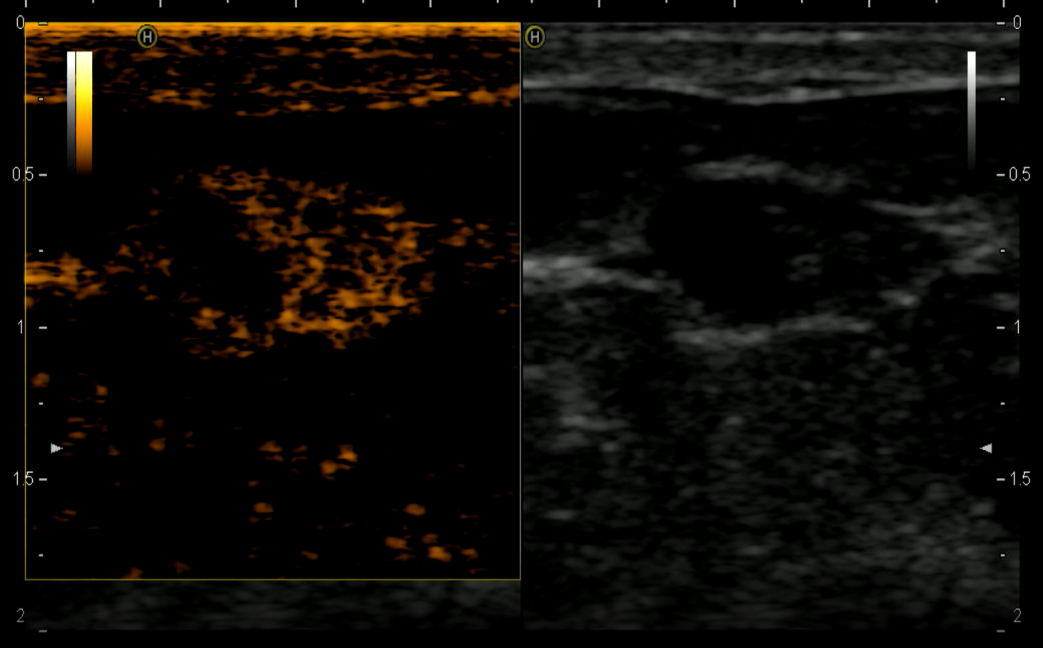
Рис.12 Ультразвуковое исследование с контрастированием: папиллома молочной железы
Используется ли УЗИ для диагностики лимфатических узлов?
УЗИ является одним из наиболее эффективных методов диагностики патологии лимфатических узлов (ЛУ). Для врача онколога важно иметь информацию о статусе ЛУ, порой это играет важную роль в выборе тактики лечения. Врач УЗИ должен осмотреть подмышечные, надключичные и подключичные ЛУ и занести информацию об их состоянии в протокол. Следует знать, что при МГ определяются только подмышечные ЛУ, которые иногда на снимке видны только частично.
Где проходить УЗИ молочных желез?
Специалисты, которые интерпретируют и МГ, и УЗИ, как правило, работают в специализированных онкологических клиниках. Анализируйте отзывы.
Магнитно-резонансная томография молочных желез
МРТ – метод диагностики, основанный на получении изображений внутренних органов с помощью радиоволн и сильного магнитного поля. Главное противопоказание к выполнению МРТ – наличие металлических конструкций в теле пациентки, в том числе кардиостимуляторов. МРТ – высокотехнологичный метод диагностики, широко применяемый за рубежом, но пока в России он редко используется для диагностики заболеваний молочных желез. Причинами являются высокая цена исследования, ограниченное число томографов в различных регионах страны и самое главное – недостаток профильных специалистов, которые правильно интерпретируют полученные МР-данные.
Показаниями для МРТ молочных желез являются высокая маммографическая плотность, наличие имплантов. Также это метод выбора у женщин с выявленной мутацией генов BRCA1 и BRCA2.
(Смотрите раздел «Факторы риска развития рака молочной железы»). В определенных случаях МРТ позволяет выявить раки, неопределяемые на МГ и УЗИ. Опытный врач-онколог или диагност знает, в каких случаях необходимо выполнение МРТ.
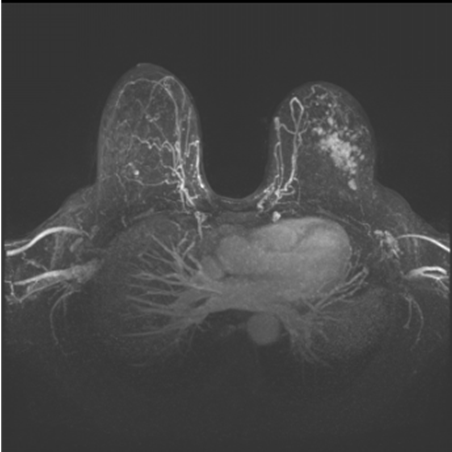
Рис.13 МР-томограмма рака молочной железы
Как проводится МРТ молочных желез?
Исследование проводится с контрастированием. Это значит, что вам в локтевую вену установят катетер и подключат к автоматизированному инжектору, через который в нужный момент введут контрастное вещество (в некоторых учреждениях введение контраста проводят вручную). У женщин репродуктивного возраста МРТ выполняется строго на 6–12 день менструального цикла. Это связано с тем, что во вторую фазу железистая ткань активно накапливает контрастное вещество, что может затруднять диагностику. После наступления менопаузы МРТ молочных желез можно проводить в любой день.
Рентген-лаборант уложит вас лицом вниз на специальную катушку с отверстиями, куда вы поместите свою грудь. Далее стол вместе с катушкой будет плавно передвигаться в тоннель томографа. Будьте готовы в таком положении пролежать около 30–40 минут. У пациенток с клаустрофобией проведение МРТ порой вызывает большие трудности.
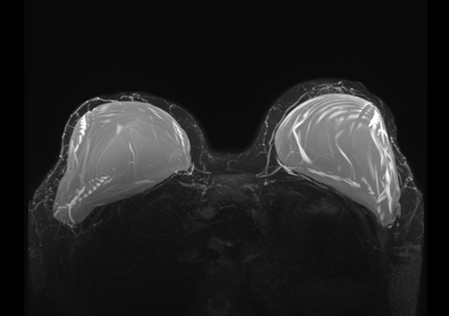
Рис.14 МР-томограмма имплантов молочной железы
При помощи МРТ проводится диагностика лимфатических узлов?
МРТ позволяет врачу-диагносту увидеть подмышечные, подключичные лимфатические узлы и даже парастернальные, которые невозможно определить при УЗИ и тем более при МГ.
Где лучше делать МРТ молочных желез?
Ответ на этот вопрос будет аналогичным – в специализированных учреждениях и у экспертов в диагностике молочных желез. Однако если вы выполните МРТ молочных желез по месту жительства, то всегда сможете отдать диски на пересмотр профильному специалисту.
Факторы риска развития рака молочной железы
К высоким факторам риска развития РМЖ относят:
- генетическую предрасположенность: мутация гена Breast Cancer 1 (BRCA1) или Breast Cancer 2 (BRCA2). Риск на протяжении жизни составляет 50–85 % у носителей мутации BRCA1 и 45 % у носителей BRCA2. Наследственный РМЖ составляет от 5 % до 10 % всех случаев;
- семейную историю РМЖ:тродственники первой степени родства, особенно перенесшие заболевание в молодом возрасте;
- лучевую терапию грудной клетки, полученную в молодом возрасте (болезнь Ходжкина). Совокупный риск составляет 20–25 % к 45 годам;
- персональную историю РМЖ (8–10-кратный риск);
- высокую маммографическую плотность молочных желез (4-кратный риск).
К среднему риску относятся:
- ранний возраст наступления менструации и поздний возраст менопаузы;
- бездетность;
- поздний возраст при рождении первого ребенка;
- длительный прием оральных контрацептивов;
- длительный прием заместительной гормональной терапии;
- частое употребление алкоголя;
- высокий индекс массы тела.
Профилактические меры, снижающие риск развития рака молочной железы:
- продолжительное грудное вскармливание;
- регулярная физическая активность;
- контроль веса;
- недопущение вредного употребления алкоголя;
- предотвращение воздействия табачного дыма;
- отказ от длительного использования гормонов;
- предотвращение чрезмерного воздействия радиации.
Система описания и протоколирования лучевых методов диагностики BI-RADS
Сегодня эталоном описания результатов ультразвукового, маммографического и магнитно-резонансного исследований молочной железы является система, разработанная Американским коллегией радиологии American College of Radiology (ACR) – Breast Imaging Reporting and Data System (BI-RADS), которая включает 7 категорий (таблица 1).
Таблица 1 – BI-RADS категории
|
Категории |
Диагноз |
|
1 |
– Нормальная ткань молочной железы – Патология не определяется – Изображение полное – Отсутствуют признаки для комментирования – Вероятность РМЖ 0 % – Направление действий: рутинное исследование |
|
2 |
– Доброкачественное образование – Изображение полное – Обнаруженные образования имеют все признаки доброкачественности – Вероятность РМЖ 0 % – Направление действий: рутинное исследование |
|
3 |
– Вероятнее доброкачественное образование – Изображение полное – Обнаруженные признаки вероятно доброкачественные – Вероятность РМЖ <2 % – Направление действий: повторное исследование через короткий интервал (3–6 месяцев) |
|
4 |
– Подозрительное образование – Обнаруженные подозрительные признаки – Вероятность РМЖ около 30 % (2–90%) – Субкатегории: 4а – низкая вероятность 4b – умеренная вероятность 4с – высокая вероятность – Направление действий: чрескожная биопсия |
|
5 |
– Высокая вероятность злокачественного образования – Изображение полное – Обнаруженные изменения имеют типичные признаки РМЖ – Вероятность РМЖ 90 % – Направление действий: чрескожная биопсия |
|
6 |
– Гистологически верифицированный РМЖ – Гистологическое заключение получено до начала лечения – Направление действий: начать лечение, предоперационная подготовка, оценка эффективности неоадъювантного лечения |
|
0 |
– Изображение неполное – Образование молочной железы нуждается в дополнительных диагностических мероприятиях – Используется при скрининге – Направление действий: завершение диагностического алгоритма |
Категории BI-RADS отражают степень вероятности наличия РМЖ. Выставленная врачом категория определяет дальнейшую диагностическую тактику, то есть маршрутизацию пациентки.
Система описания BI-RADS направлена на стандартизированный подход в описании характеристик медицинского лучевого изображения патологии молочной железы, что позволяет докторам разных дисциплин и разных стран говорить на одном языке.
Если вы получили заключение без категории BI-RADS, скорее всего, его писал врач-диагност общего профиля, который не знаком с тонкостями диагностики заболеваний молочных желез.
Как часто нужно наблюдаться?
В разных странах есть свои модели обследования молочных желез, так называемые чекапы (check up). Ниже я привожу усредненную информацию, основанную больше на клинической необходимости, а не на экономической целесообразности.
Если у вас нет факторов риска развития РМЖ и вам уже исполнилось 40 лет, то следует проходить МГ раз в 2 года, а УЗИ (при наличии высокой маммографической плотности молочных желез) раз в год. До 40 лет методом выбора будет УЗИ.
Если у вас есть наследственные факторы риска (мутация гена BRCA 1 или 2), то в данном случае мировые ассоциации (American College of Radiology, American Cancer Society and Society of Breast Imaging) рекомендуют ежегодно проходить МРТ молочных желез.
American College of Radiology (ACR) рекомендует маммографию у женщин из группы высокого риска начинать раньше – в 30-летнем возрасте.
Причем на 10 лет раньше, чем заболевший родственник на момент постановки диагноза.
Ежегодная МРТ молочной железы с контрастным усилением используется как дополнительный метод скрининга к маммографии.
Это увеличивает уровень выявления рака. У носителей мутации BRCA чувствительность МРТ составила 90 % по сравнению с 37,5 % – для МГ и УЗИ.
Биопсия – взятие материала для гистологического исследования
Если в заключении, которое вам выдали после выполнения диагностического метода молочных желез, фигурирует категория BI-RADS 4 или 5, то необходимо провести биопсию, то есть взятие столбика ткани для дальнейшего гистологического исследования. Следует помнить, что заключение лучевой диагностики является предположительным, а диагноз ставится только после гистологического анализа образцов ткани. В медицинской практике используется три варианта чрескожного взятия материала:
- тонкоигольная аспирационная пункционная биопсия (ТАПБ),
- трепан-биопсия (ТБ),
- вакуум ассистированная биопсия (ВАБ).
При этом используются три метода навигации иглы в зависимости от степени визуализации объекта:
- стереотаксический (рентгенологический),
- ультразвуковой,
- магнитно-резонансный.
В онкологической практике в 90 % случаев используется ТБ под ультразвуковым наведением, отличающаяся высокой эффективностью, простотой исполнения, экономичностью по сравнению с рентгенологическим стереотаксическим и МРТ наведением.
При скоплении микрокальцинатов, подозрительных на РМЖ (около 11 % всех случаев), производится стереотаксическая биопсия под рентгеновским контролем, ее еще называют маммотест.
В 3 % случаев для определения распространенности процесса, визуализируемого только при МРТ, материал берется с помощью ВАБ под контролем МРТ.
ТАПБ используется только для взятия цитологического материала из подозрительных лимфатических узлов (ЛУ) или в случае аспирации содержимого кист или других жидкостных структур молочной железы.
ВАБ в последнее время чаще используется для малоинвазивного удаления фиброаденом под ультразвуковым контролем. Следует знать, что перед удалением любого образования необходимо гистологически или цитологически подтвердить, что оно доброкачественное.
Биопсию назначает врач-онколог на основании заключения лучевой визуализации и клинических данных, а вот метод для навигации иглы может рекомендовать врач лучевой диагностики.
Не следует бояться. Сейчас, как правило, биопсия выполняется под местной анестезией.
Что можно узнать из результатов биопсии?
После выполнения биопсии врач-патоморфолог исследует образцы тканей под микроскопом в поисках атипичных или раковых клеток.
Исследование может занять одну или две недели. Врач определяет, является ли подозрительная область злокачественной.
Для пациента ожидание результатов может быть настоящей проблемой, но возможность принять обоснованное решение относительно вашего лечения того стоит.
Если раковые клетки не обнаружены, в отчете будет указано, что клетки в опухоли доброкачественные. Тем не менее, некоторые виды доброкачественных образований требуют определенного последующего наблюдения или лечения.
Если раковые клетки будут обнаружены, в отчете будет предоставлена дополнительная информация, которая поможет определить дальнейшее лечение. Отчет о биопсии также будет включать тип опухоли и скорость или степень роста опухоли. Если обнаружен рак, врач-патоморфолог также проведет лабораторные тесты, чтобы проверить клетки на наличие рецепторов эстрогена или прогестерона.
Гистологическое заключение поможет вашему врачу определиться с дальнейшими шагами. Скорее всего, вам может потребоваться дообследование.
Врач использует гистологическое заключение и результаты методов лучевой диагностики для определения стадии рака и разработки наилучшего плана лечения для вас.
Заключение
Раннее выявление рака молочной железы – сложная и важная проблема современной медицины. Казалось бы, что может быть сложного в диагностике молочных желез, но индивидуальное строение желез у каждой женщины и большое разнообразие патологических изменений крайне затрудняют работу врачу-диагносту. В определенных случаях доброкачественные и злокачественные образования похожи между собой, и чтобы не пропустить рак, врач должен владеть несколькими методами диагностики – быть мультимодальным специалистом. Обилие информации в интернете иногда только запутывают женщину, которая впервые столкнулась с данной проблемой. Доверяйте только проверенным источникам.
Глоссарий
- ВАБ – вакуум ассистированная биопсия
- ВМП – высокая маммографическая плотность
- ГЗ – гистологическое заключение
- КСМГ – контрастная спектральная маммография
- ЛУ – лимфатические узлы
- МРТ – магнитно-резонансная томография
- РМЖ – рак молочной железы
- СЭГ — соноэластография
- ТАПБ – тонкоигольная аспирационная пункционная биопсия
- ТБ – трепан-биопсия
- УЗИ — ультразвуковое исследование
- ЦМГ – цифровая маммография
- ЦТ – цифровой томосинтез
- ACR – American college of radiology (американская коллегия радиологов)
- BI-RADS – breast imaging and reports data system (система интерпретации и протоколирования визуализации молочной железы)
- BRCA – breast cancer gene (гены рака молочной железы)
Список литературы
- Семиглазов, В. Ф. Рекомендации для врачей̆ по ведению пациентов с раком молочной железы / В. Ф. Семиглазов, П. В. Криворотько, В. В. Семиглазов, Г. А. Дашян, Р. М. Палтуев // Приложение к журналу «Медицинский совет». ‒ 2017. ‒ № 14. ‒ C. 239.
- Семиглазов, В. Ф. Эпидемиология и скрининг рака молочной железы / В. Ф. Семиглазов, В. М. Мерабишвили, В. В. Семиглазов, А. В. Комяхов, Е. В. Демин, А. В. Атрощенко, М. В. Харитонов // Вопросы онкологии. – 2017. – № 63(3). – С. 375-384.
- Семиглазов, В. Ф. Рак молочной железы: мультидисциплинарный подход к лечению / В. Ф. Семиглазов // Практическая онкология. ‒ 2015. ‒ T. 16, № 2. ‒ C. 49-54.
- Мерабишвили, В. М. Эпидемиология и выживаемость мужчин – больных раком молочной̆ железы / В. М. Мерабишвили // Вопросы онкологии. ‒ 2016. ‒ T. 62. ‒ C. 245-252.
- Рожкова, Н. И. Новые возможности лучевых технологий при рентгенонегативном раке / Н. И. Рожкова, А. Д. Каприн, И. И. Бурдина, С. Б. Запирова, М. Л. Мазо, С. П. Прокопенко, О. Э. Якобс, Ф. Н. Михайлович // Медицинская наука и образование Урала. ‒ 2019. – № 2/98. ‒ C. 36-41.
- Семиглазов, В. В. Диагностика и лечение рака молочной железы in situ. Клинические рекомендации российского общества онкомаммологов / В. В. Семиглазов // Опухоли женской репродуктивной системы. ‒ 2017. ‒ №. 13. ‒ C. 41-56.
- Рожкова, Н. И. Новые возможности лучевых технологий при рентгенонегативном раке / А. Д. Каприн, И. И. Бурдина, С. Б.Запирова, М. Л. Мазо, С. П. Прокопенко, Н. М. Федоров // Медицинская наука и образование Урала. ‒ 2019. ‒ T. 20(2). С. 36-41.
- Рожкова, Н. И. Онкомаммоскрининг в реализации программ активного долголетия / Н. И. Рожкова, И. И. Бурдина, С. Б. Запирова, А. Д. Каприн, П. Г. Лабазанова, М. Л. Мазо, С. Ю. Микушин, С. П. Прокопенко, О. Э. Якобс // Академический журнал Западной Сибири. ‒ 2019. ‒ №. 15 (2). ‒ C. 3-5.
- Бусько Е.А. Оптимизация диагностики непальпируемых образований молочной железы / В.В. Семиглазов, Е.А. Бусько, А.Н. Зайцев, И.И. Семенов // Вопросы онкологии. − 2009. − №3. − С. 387-388.
- Бусько Е.А. Возможности соноэластографии в диагностике опухолей молочных желез размерами до 2 см / Е.А. Бусько, И.И. Семенов, В.В. Семиглазов // Вопросы онкологии. − 2012. − № 3-vol-58. − С.359-362.
URL: http://www.fesmu.ru/elib/Article.aspx?id=262217 - Бусько Е.А. Определение порогового значения соноэластографического коэффициента жесткости в дифференциальной диагностике доброкачественных и злокачественных образований молочной железы / Е.А. Бусько, А.В. Мищенко, В.В. Семиглазов // Кремлевская медицина. Клинический вестник. − 2013. − №1 – С. 112-115. URL: http://unmc.su/wp-content/uploads/2013/01/Journal-1-2013.pdf.
- Бусько Е.А. Дифференциальная ультразвуковая и соноэластографическая диагностика долькового рака молочной железы / Е.А. Бусько, Т.Т. Табагуа, А.В. Мищенко, В.В. Семиглазов // Ученые записки. − 2013. − Том XX № 2 − С. 45-49.
- Бусько Е.А. Эффективность УЗИ и соноэластографии в диагностике непальпируемых и пальпируемых образований молочной железы / Е.А. Бусько, А.В. Мищенко, В.В. Семиглазов, Т.Т. Табагуа // Вопросы онкологии. − 2013. − № 3 − С. 375-381. URL: http://www.fesmu.ru/elib/Article.aspx?id=279709.
- Бусько Е.А. Изменение соноэластографических показателей жесткости как критерий оценки эффективности неоадъювантной химиотерапии рака молочной железы / Е.А. Бусько, Т.Ю. Семиглазова, В.В. Клименко [и др.] // Ученые записки. − 2014. −№ 1. − С. 62-67.
- Бусько Е.А. Корреляция соноэластографических показателей жесткости со степенью патоморфологического регресса местно-распространенного рака молочной железы на фоне неоадъювантной химиотерапии / Е.А. Бусько, А.В. Мищенко, В.В. Семиглазов, П.В. Криворотько, Т.Ю. Семиглазова, Р.М. Палтуев, А.С. Петрова, А.В. Комяхов, В.Ф. Семиглазов // Опухоли женской репродуктивной системы, 2017- Том 12, № 4 С. 25-31 DOI: 10.17650/1994-4098-2016-12-4-25-31
- Бусько Е.А. Паттерны контрастного ультразвукового исследования молочной железы / Е.А. Бусько /Радиология и практика. 2017. № 4 (64). С. 6-17
- Бусько Е.А. Возможности ультразвукового цветового допплеровского картирования в ранней диагностике рака молочной железы / Е.А. Бусько, В.В. Семиглазов, А.В. Мищенко, А.С. Шишова, В.О. Смирнова, Е.В. Костромина, А.В. Черная, А.С. Артемьева, П.В. Криворотько / Сибирский онкологический журнал 2019. Т. 18. № 6. С. 12-19.
DOI: 10.21294/1814-4861-2019-18-6-12-19 - Бусько Е.А. Эффективность мультипараметрического ультразвукового исследования с применением компрессионной эластографии в ранней диагностике образований молочной железы / Е.А. Бусько, В.В. Семиглазов, А.В. Мищенко, К.В. Козубова, А.С. Шишова, М.И. Арабачян, Е.В. Костромина, П.В. Криворотько / Лучевая диагностика и терапия 2019. № 4(10). С. 6-13.
DOI: 10.22328/2079-5343-2019-10-4-6-13 - Бусько Е.А. Модель системы принятия диагностических решений на основе мультипараметрических ультразвуковых показателей образований молочной железы / Бусько Е. А., Гончарова А. Б., Рожкова Н.И., Семиглазов В.В., Шишова А.С., Жильцова Е.К., Зиновьев Г., Белобородова К., Криворотько П.В. // Вопросы онкологии 2020 Т. 66 № 6 С. 653-658
DOI: 10.37469/0507-3758-2020-66-6-653-658 - Бусько Е.А. Использование статистического метода псевдорандомизации в сравнительной оценке диагностической эффективности методов медицинской визуализации на примере магнитно резонансной томографии и контрастно-усиленного ультразвукового исследования / Е. А. Бусько, А. Б. Гончарова, Д. А. Бучина, А. С. Натопкина // Опухоли женской репродуктивной системы. 2021. Том 17 № 3. С. 37-43. DOI: 10.17650/1994-4098-2021-17-3
- Ульянова Р.Х. Дифференциальная диагностика патологии молочной железы с помощью типов накопления контрастного препарата при контрастной спектральной двуэнергетической маммографии. Ульянова Р.Х., Чёрная А.В., Криворотько П.В., Новиков С.Н., Канаев С.В., Артемьева А.С., Шевкунов Л.Н., Тятьков С.А., Данилов В.В. // Вопросы онкологии. 2020. Т. 66. № 3. С. 252-261.
- Черная А.В. Маммография и маммосцинтиграфия с 99М TC-MIBI в диагностике мультицентричного рака молочной железы / Черная А.В., Канаев С.В., Новиков С.Н., Крживицкий П.И., Криворотько П.В., Артемьева А.С., Попова Н.С., Бусько Е.А., Шумакова Т.А., Башлык В.О. // Вопросы онкологии. 2017. Т. 63. № 6. С. 876-881.
- Tabar, L. Effect of Mammography Screening on Mortality by Histological Grade / L. Tabar, T. H.-H. Chen, A. M.-F. Yen, S. L.-S. Chen, J. C.-Y. Fann, S. Y.-H. Chiu, M. M. S. Ku, W. Y.-Y. Wu, C.-Y. Hsu, Y.-Y. Chen, B K. Eckmann, R. A. Smith, S. W. Duffy // Cancer Epidemiology Biomarkers & Prevention. ‒ 2018. ‒ Vol. 27, № 2. ‒ P. 154-157.
- Tabar, L. The incidence of fatal breast cancer measures the increased effectiveness of therapy in women participating in mammography screening / L. Tabar, P. B. Dean, T. H.-H. Chen, A. M.-F. Yen, S. L.-S. Chen, J. C.-Y. Fann, S. Y.-H. Chiu, M. M.-S. Ku, W. Y.-Y. Wu, C.-Y. Hsu, Y.-C. Chen, K. Beckmann, R. A. Smith, S. W. Duffy // Cancer. ‒ 2019. ‒ Vol. 125, № 4. ‒ P. 515-523.
- Harbeck, N. Breast cancer / N. Harbeck, M. Gnant // Lancet. ‒ 2017. ‒ Vol. 389, № 10074. ‒ P. 1134-1150.
- Mercado, C. L. BI-RADS Update / C. L. Mercado // Radiologic Clinics of North America. ‒ 2014. ‒ Vol. 52, № 3. ‒ P. 481–487.
- D’Orsi, C.J. ACR BI-RADS® Atlas, Breast Imaging Reporting and Data System / C.J. D’Orsi, E.A. Sickles, E.B. Mendelson [et. al.]. ‒ Reston, VA, American College of Radiology, 2013.
- Elezaby, M. ACR BI-RADS Assessment Category 4 Subdivisions in Diagnostic Mammography: Utilization and Outcomes in the National Mammography Database / M. Elezaby, G. Li, M. Bhargavan-Chatfield, E. S. Burnside, W. B. DeMartini // Radiology. ‒ 2018. ‒ Vol. 287, № 2. ‒ P. 416-422.
- Hu, Y. Does patient age affect the PPV3 of ACR BI-RADS Ultrasound categories 4 and 5 in the diagnostic setting? / Y. Hu, Y. P. Yang, R. Gu, L. Jin, S. Y. Shen, F. T. Liu, H. L. Wang, J. S. Mei, X. F. Jiang, Q. Liu, F. X. Su // European Radiology. ‒ 2018. ‒ Vol. 28, № 6. ‒ P. 2492-2498.
- Rawashdeh, M. Breast lesion shape and margin evaluation: BI-RADS based metrics understate radiologists’ actual levels of agreement / M. Rawashdeh, S. Lewis, M. Zaitoun, P. Brennan // Computers in Biology and Medicine. ‒ 2018. ‒ Vol. 96. ‒ P. 294-298.
- Hofvind, S. Digital Breast Tomosynthesis and Synthetic 2D Mammography versus Digital Mammography: Evaluation in a Population-based Screening Program / S. Hofvind, T. Hovda, A. S. Holen, C. I. Lee, J. Albertsen, H. Bjorndal, S. H. B. Brandal, R. Gullien, J. Lomo, D. Park, L. Romundstad, P. Suhrke, E. Vigeland, P. Skaane // Radiology. ‒ 2018. ‒ Vol. 287, № 3. ‒ P. 787-794.
- Boisserie-Lacroix, M. The new 2013 BI-RADS ACR MRI Lexicon / M. Boisserie-Lacroix, V. Catena, M. P. Depetiteville // Imagerie De La Femme. ‒ 2017. ‒ Vol. 27, № 1. ‒ P. 16-24.
- Vlahiotis, A. Analysis of utilization patterns and associated costs of the breast imaging and diagnostic procedures after screening mammography / A. Vlahiotis, B. Griffin, A. T. Stavros, J. Margolis // Clinicoeconomics and Outcomes Research. ‒ 2018. ‒ Vol. 10. ‒ P. 157-167.
- Grabler, P. Recall and Cancer Detection Rates for Screening Mammography: Finding the Sweet Spot / P. Grabler, D. Sighoko, L. L. Wang, K. Allgood, D. Ansell // American Journal of Roentgenology. ‒ 2017. ‒ Vol. 208, № 1. ‒ P. 208-213.
- Рожкова, Н. И. Новые возможности лучевых технологий при рентгенонегативном раке / А. Д. Каприн, И. И. Бурдина, С. Б.Запирова, М. Л. Мазо, С. П. Прокопенко, Н. М. Федоров // Медицинская наука и образование Урала. ‒ 2019. ‒ T. 20(2). С. 36-41.
- Allen, J. D. Follow-up of abnormal screening mammograms among low-income ethnically diverse women: Findings from a qualitative study / J. D. Allen, R. C. Shelton, E. Harden, R. E. Goldman // Patient Education and Counseling. ‒ 2008. ‒ Vol. 72, № 2. ‒ P. 283-292.
- Chae, E. Y. Reassessment and Follow-Up Results of BI-RADS Category 3 Lesions Detected on Screening Breast Ultrasound / E. Y. Chae, J. H. Cha, H. J. Shin, W. J. Choi, H. H. Kim // American Journal of Roentgenology. ‒ 2016. ‒ Vol. 206, № 3. ‒ P. 666-672.
- Ong, M. S. National Expenditure For False-Positive Mammograms And Breast Cancer Overdiagnoses Estimated At $4 Billion A Year / M. S. Ong, K. D. Mandl // Health Affairs. ‒ 2015. ‒ Vol. 34, № 4. ‒ P. 576-583.
- Brem, R. F. Assessing Improvement in Detection of Breast Cancer with Three-dimensional Automated Breast US in Women with Dense Breast Tissue: The Somoinsight Study / R. F. Brem, L. Tabar, S. W. Duffy, M. F. Inciardi, J. A. Guingrich, B. E. Hashimoto, M. R. Lander, R. L. Lapidus, M. K. Peterson, J. A. Rapelyea, S. Roux, K. J. Schilling, B. A. Shah, J. Torrente, R. T. Wynn, D. P. Miller // Radiology. ‒ 2015. ‒ Vol. 274, № 3. ‒ P. 663-673.
- Wanders, J. O. P. Volumetric breast density affects performance of digital screening mammography / J. O. P. Wanders, K. Holland, W. B. Veldhuis, R. M. Mann, R. M. Pijnappel, P. H. M. Peeters, C. H. van Gils, N. Karssemeijer // Breast Cancer Research and Treatment. ‒ 2017. ‒ Vol. 162, № 1. ‒ P. 95-103.
- Wengert, G. J. Multimodality Imaging of Breast Parenchymal Density and Correlation with Risk Assessment / G. J. Wengert, T. H. Helbich, D. Leithner, E. A. Morris, P. A. T. Baltzer, K. Pinker // Current Breast Cancer Reports. ‒ 2019. ‒ Vol. 11, № 1. ‒ P. 23-33.
- Abdikenov, B. Analytics of Heterogeneous Breast Cancer Data Using Neuroevolution / B. Abdikenov, Z. Iklassov, A. Sharipov, S. Hussain, P. K. Jamwal // Ieee Access. ‒ 2019. ‒ Vol. 7. ‒ P. 18050-18060.
- Brancati, N. A Deep Learning Approach for Breast Invasive Ductal Carcinoma Detection and Lymphoma Multi-Classification in Histological Images / N. Brancati, G. De Pietro, M. Frucci, D. Riccio // Ieee Access. ‒ 2019. ‒ Vol. 7. ‒ P. 44709-44720.
- Harvey, H. The Role of Deep Learning in Breast Screening / H. Harvey, E. Karpati, G. Khara, D. Korkinof, A. Ng, C. Austin, T. Rijken, P. Kecskemethy // Current Breast Cancer Reports. ‒ 2019. ‒ Vol. 11, № 1. ‒ P. 17-22.
- Jadoon, M. M. Three-Class Mammogram Classification Based on Descriptive CNN Features / M. M. Jadoon, Q. Zhang, I. Ul Haq, S. Butt, A. Jadoon // Biomed Research International [Электронный ресурс]. ‒ Vol. 2017. – Article ID 3640901. – 11 p. – URL: https://doi.org/10.1155/2017/3640901.
- Kim, E.-K. Applying Data-driven Imaging Biomarker in Mammography for Breast Cancer Screening: Preliminary Study / E.-K. Kim, H.-E. Kim, K. Han, B. J. Kang, Y.-M. Sohn, O. H. Woo, C. W. Lee // Scientific Reports. ‒ 2018. ‒ Vol. 8 (1). – 11 p. – Article number: 2762.
- Kurek, J. Barhoumi W. Deep learning versus classical neural approach to mammogram recognition / J. Kurek, B. Swiderski, S. Osowski, M. Kruk // Bulletin of the Polish Academy of Sciences-Technical Sciences. ‒ 2018. ‒ Vol. 66, № 6. – P. 831–840.
- Lamy, J.-B. Explainable artificial intelligence for breast cancer: A visual case-based reasoning approach / J.-B. Lamy, B. Sekar, G. Guezennec, J. Bouaud, B. Seroussi // Artificial Intelligence in Medicine. ‒ 2019. ‒ Vol. 94. ‒ P. 42-53.
- Li, Y. Classification of Breast Cancer histology Images Using Multi-Size and Discriminative Patches Based on Deep Learning / Y. Li, J. Wu, Q. Wu // Ieee Access. ‒ 2019. ‒ Vol. 7. ‒ P. 21400-21408.
- Mohamed, A. A. A deep learning method for classifying mammographic breast density categories / A. A. Mohamed, W. A. Berg, H. Peng, Y. Luo, R. C. Jankowitz, S. Wu // Medical Physics. ‒ 2018. ‒ Vol. 45, № 1. ‒ P. 314-321.
- Ragab, D. A. Breast cancer detection using deep convolutional neural networks and support vector machines / D. A. Ragab, M. Sharkas, S. Marshall, J. Ren // Peerj. ‒ 2019. ‒ Vol. 7. – 19 p.
- Ribli, D. Detecting and classifying lesions in mammograms with Deep Learning / D. Ribli, A. Horvath, Z. Unger, P. Pollner, I. Csabai // Scientific Reports. ‒ 2018. ‒ Vol. 8 (1).
- Wu, G.-G. Artificial intelligence in breast ultrasound / G.-G. Wu, L.-Q. Zhou, J.-W. Xu, J.-Y. Wang, Q. Wei, Y.-B. Deng, X.-W. Cui, C. F. Dietrich // World Journal of Radiology. ‒ 2019. ‒ Vol. 11, № 2. ‒ P. 19-25.
Под редакцией: главного внештатного онколога Северо-Западного федерального округа, профессора, д.м.н. Беляева Алексея Михайловича
В создании данного материала принимали участие ведущие эксперты РФ в диагностике и лечении рака молочной железы:
- член-кор. РАН, профессор, д.м.н. Семиглазов Владимир Федорович
- профессор, д.м.н. Семиглазов Владислав Владимирович
- профессор, д.м.н. Криворотько Петр Владимирович
- доцент, д.м.н. Багненко Сергей Сергеевич
- к.м.н. Табагуа Тенгиз Тенгизович
- к.м.н. Артемьева Анна Сергеевна
Что вам необходимо сделать
Если вы хотите узнать побольше о бесплатных возможностях ФБГУ НМИЦ онкологии им. Н.Н. Петрова Минздрава России, получить очную или заочную консультацию по диагностике и лечению, записаться на приём, ознакомьтесь с информацией на официальном сайте.
Если вы хотите общаться с нами через социальные сети, обратите внимание на аккаунты в ВКонтакте и Одноклассники.
Если вам понравилась статья:
- оставьте комментарий ниже;
- поделитесь в социальных сетях через удобные кнопки: