Злокачественные новообразования скелета — это состояние, при котором в кости появляются атипичные клетки, обладающие возможностью бесконтрольного роста и деления.
Первичные новообразования костей являются одними из самых редких опухолей человека и составляют всего 1% от всех ЗНО. Чаще возникает метастатическое поражение костей при других злокачественных заболеваниях, таких как рак молочной железы, легкого и т.д.
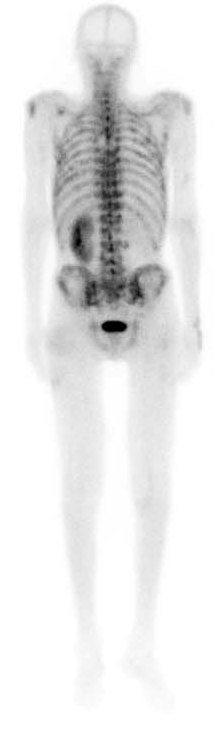
Фото: Остеосцинтиграфия при метастатическом поражение костей скелета
Наиболее частыми подтипами опухолей костей являются остеогенные саркомы, саркомы семейства Юинга и хондросаркомы.
Сарко́ма (лат. sarcoma; от др.-греч. σάρξ — «плоть», «мясо» + лат. ōma — «опухоль») — группа злокачественных опухолей соединительной ткани: костной, хрящевой, мышечной, жировой, стенок кровеносных и лимфатических сосудов, нервов и т.д.
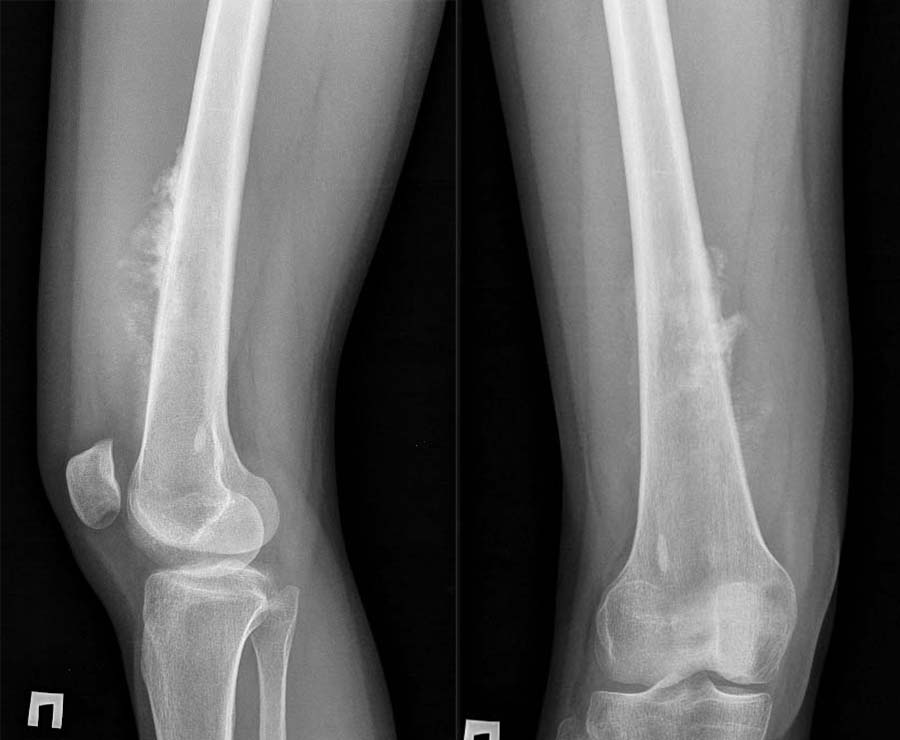
Фото: Rg при остеогенной саркоме бедренной кости
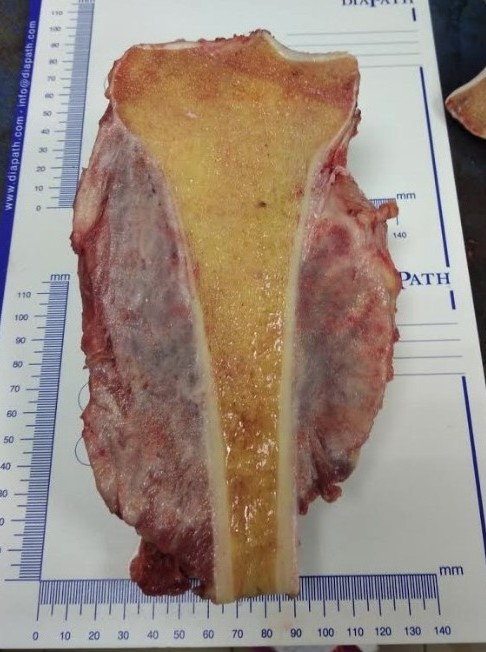
Фото: Остеогенная саркома, патологоанатомический препарат
Примерно 50% костных сарком диагностируется в возрасте до 35 лет, основными пиками заболеваемости является второе и третье десятилетие жизни.
В настоящее время описано не менее 70 подвидов данного заболевания. Это обуславливает тот факт, что заниматься диагностикой и лечением столь редкой патологии должны лишь в профильных референсных онкологических центрах.
Кроме того, для постановки диагноза необходима слаженная работа мультидисциплинарной команды: клиницистов, врачей лучевой диагностики и патоморфологов.
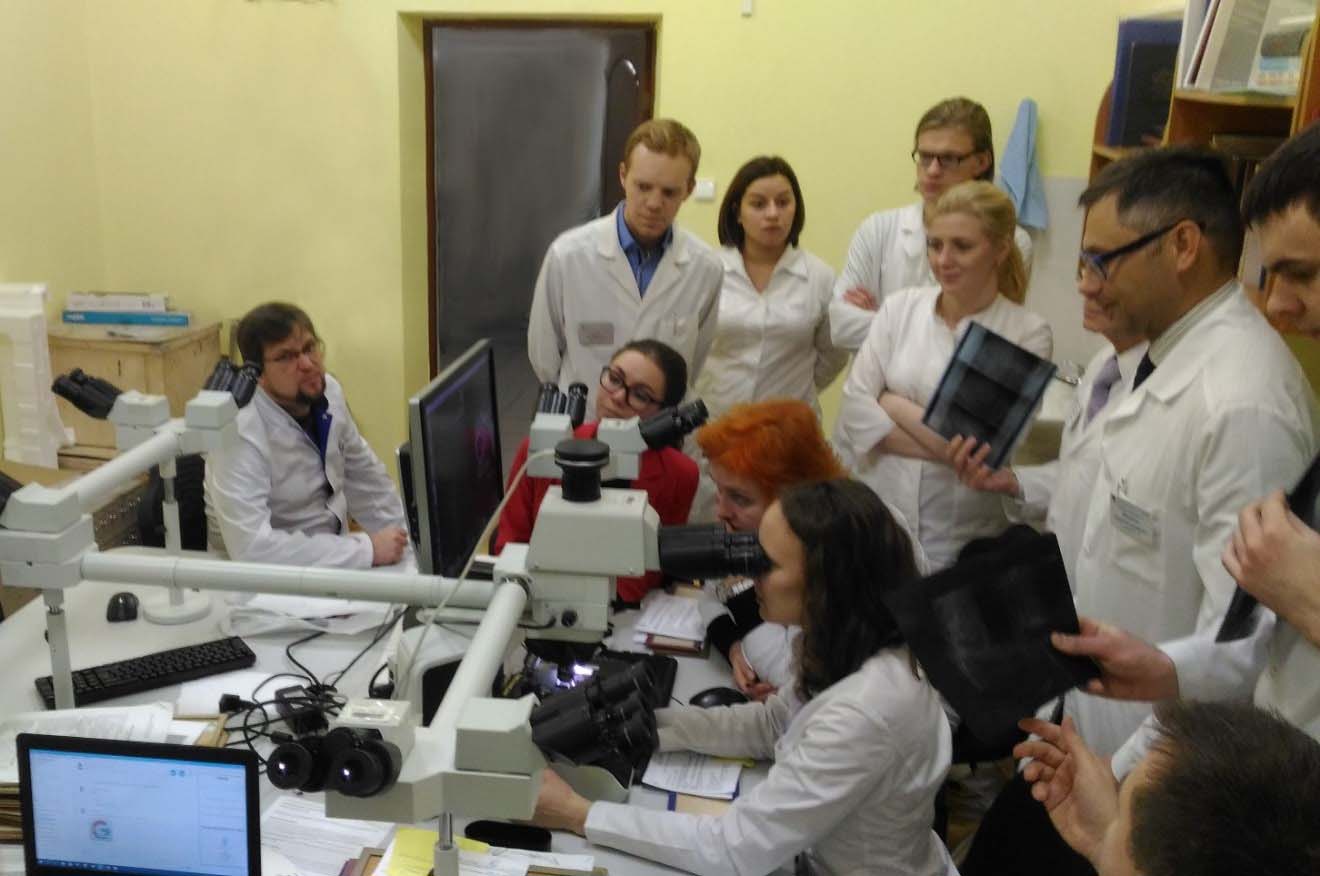
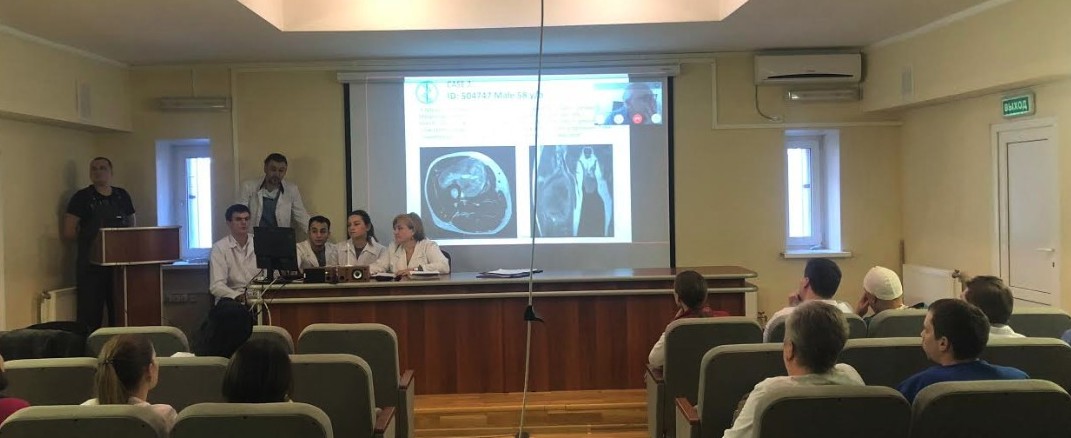

Фото: Обсуждение клинического случая на заседании мультидисциплинарной команды НМИЦ Онкологии имени Н.Н.Петрова
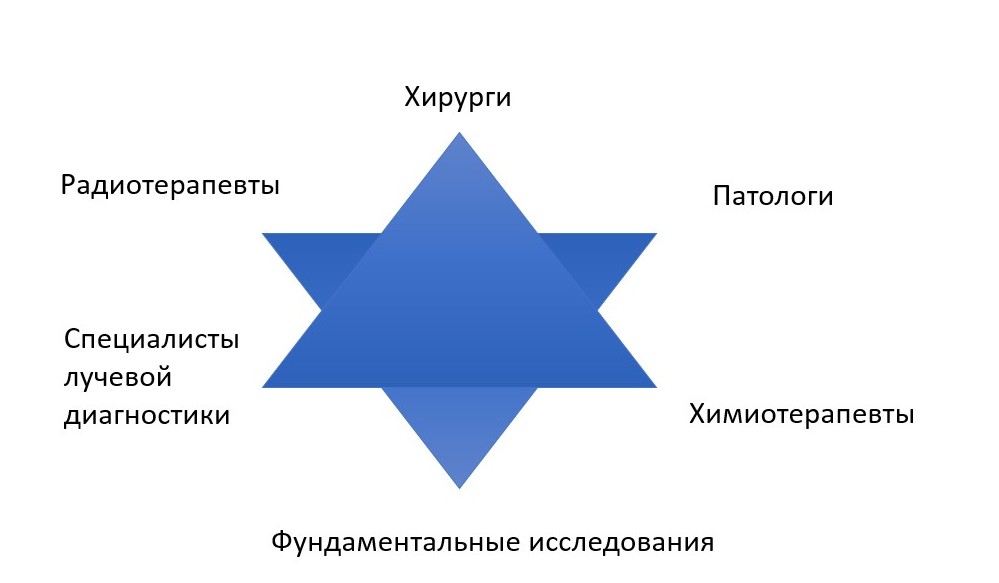
Фото: Мультидисциплинарный подход в лечении и диагностике пациентов с ЗНО костей
Диагностика данной патологии состоит из нескольких этапов. Первым является сбор анамнеза и истории заболевания при клиническом осмотре онколога. Затем выполнение различных лучевых методов визуализации: рентгенографии, ультразвукового исследования, компьютерной и магнитно-резонансной томографии, сцинтиграфии, а иногда и протонно-эмиссионной томографии.
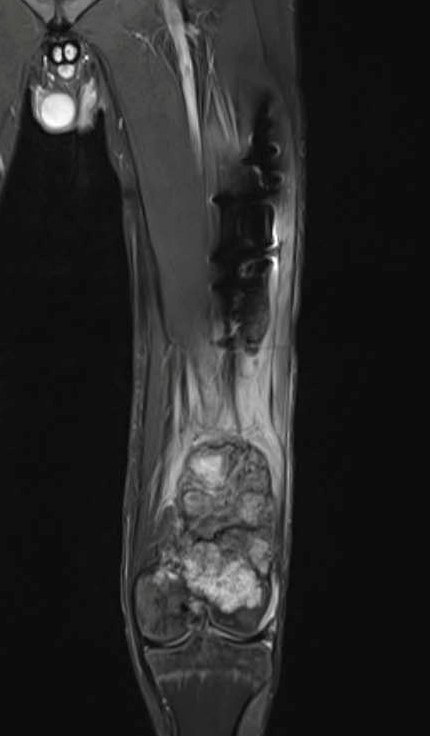
Фото: МРТ остеогенная саркома нижней трети левой бедренной кости
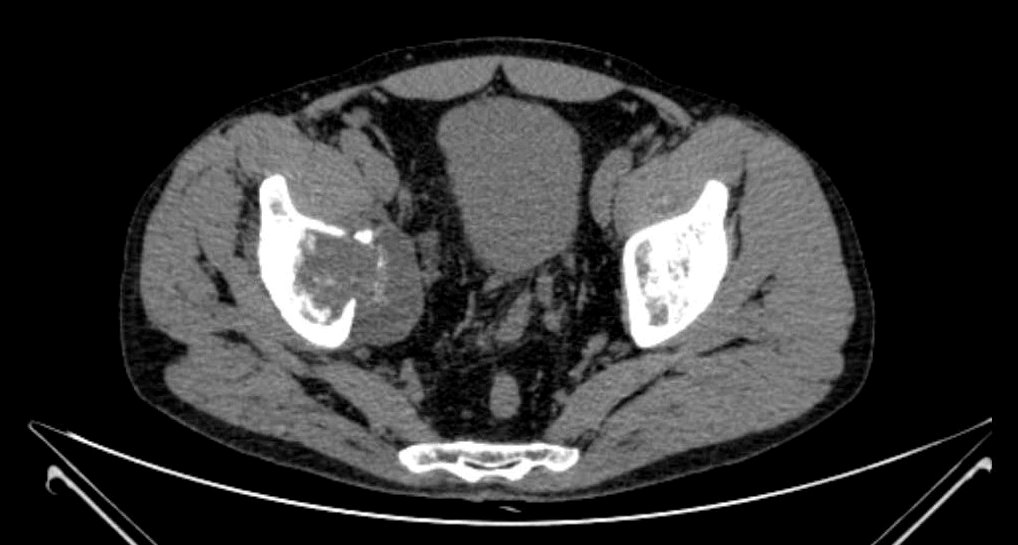
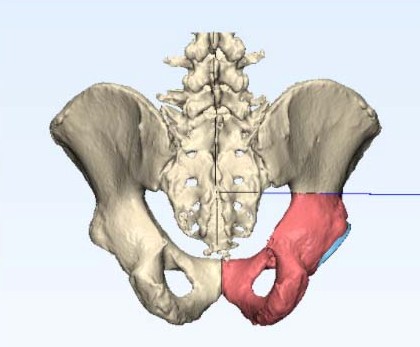
Фото: КТхондросаркома вертлужной впадины правой подвздошной кости
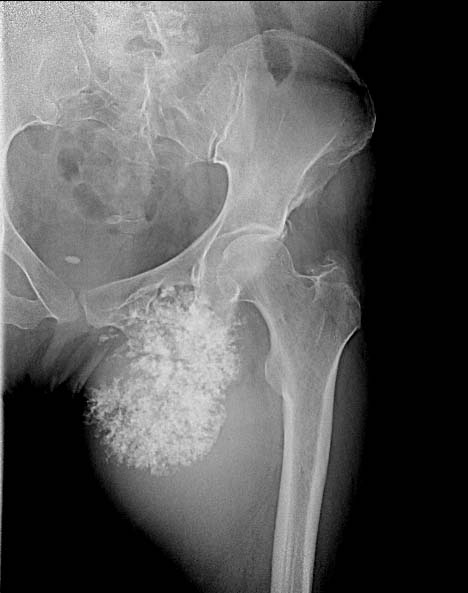
Фото: Рентгенограмма костей таза. Остеогенная саркома седалищной кости
Выполнение лишь одного метода визуализации не позволяет достаточно оценить данную патологию, например, рентгенография и компьютерная томография позволяют детально оценить изменение костной ткани, однако из-за специфики оптических свойств не дают полного представления о мягкотканных структурах и распространении по костномозговому каналу, что требует выполнения магнитно-резонансной томографии. Оценить распространение заболевания в целом позволяет применение различных методов радионуклидной диагностики – остеосцинтиграфии, ОФЭКТ и ПЭТ компьютерной томографии.
После анализа полученных данных принимается решение о целесообразности проведения биопсии новообразования.
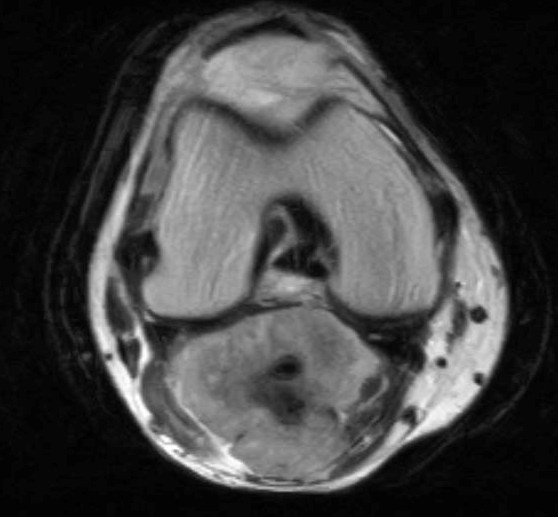
Фото: МРТ коленного сустава. Показано взаимоотношение новообразования с сосудами
Биопси́я (от др.-греч. βίος — жизнь + ὄψις — внешний вид) — метод исследования, при котором проводится прижизненный забор клеток или тканей (биоптата) опухоли из организма с диагностической целью. Без морфологического диагноза (микроскопической оценки ткани опухоли) невозможна постановка клинического диагноза, следовательно, и назначение лечения.

Фото: аппарат для трепан-биопсии

Фото: игла для костной биопсии
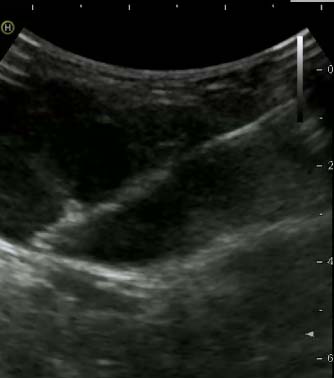
Фото: Трепан-биопсия новообразования под УЗ-навигацией
С целью постановки диагноза опухоли кости рекомендовано применение трепан-биопсии (с помощью специального устройства и биопсийной иглы через прокол кожи и окружающих опухоль тканей производят забор столбиков ткани опухоли) и инцизионной биопсии (через разрез кожи и окружающих тканей удаляется фрагмент опухоли). При выполнении трепан-биопсии применяют различные способы навигации: ультразвук, рентгенография, компьютерная томография.
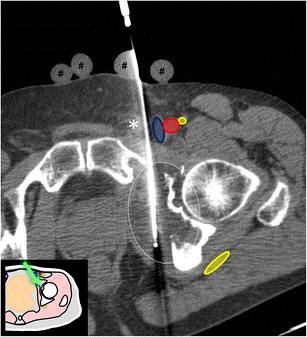
Фото: Трепан-биопсия новообразования под КТ-навигацией
При выполнении биопсии, как и при любой инвазивной процедуре, существуют определенные риски для здоровья, их стоит обсудить с лечащим врачом.
Полученный биопсийный материал (ткань опухоли) отправляют на гистологическое исследование.

Фото: Материал биопсии
Морфологическая картина различных опухолей костей и мягких тканей может быть сходной. Лишь сопоставление клинических, морфологических (в том числе и иммуногистохимических), а также данных лучевых методов визуализации позволяет в полной мере оценить опухолевый процесс для постановки корректного клинического диагноза.
Основной метод лечения опухолей костей – хирургический, но далеко не всегда единственный и применяющийся на первом этапе. При определенных подтипах опухоли необходимой первой линией лечения является химиотерапия, лучевая терапия или их комбинация. Краеугольным камнем в выборе тактики лечения является морфологический подтип опухоли, таким образом, правильный диагноз = корректное лечение.
Сейчас принятая тактика терапии больных с локализованной остеогенной саркомой подразумевает комбинированное лечение, которое включает:
- химиотерапию в качестве подготовки к операции;
- хирургическое вмешательство;
- послеоперационную химиотерапию.
Одна лишь операция нецелесообразна, потому что в 80-90 % случаев в течение 1,5 лет после нее обнаруживаются локальные рецидивы и метастазы в легких. Являясь частью комплексного лечения, химиотерапия значительно повышает показатели 5-летней выживаемости у пациентов с локализованной патологией – от 20 % до 60 %.
Основные преимущества предоперационной химиотерапии – это:
- возможность оценки того, насколько активны химиотерапевтические препараты;
- облегчение проведения хирургического вмешательства.
Перед операцией обычно проводится от 2 до 4 циклов химиотерапии. Если получен выраженный ответ опухоли на терапию – некроз новообразования 90 % и больше, – то есть большая вероятность повышения общей и безрецидивной выживаемости.
Следующий этап – операция. В первую очередь нужно рассматривать возможность проведения органосохраняющих вмешательств. Применение модульных систем эндопротезирования является самым актуальным и современным методом терапии костных сарком. Однако такой вид лечения должен проводиться только в специализированных крупных стационарах онкологического профиля, где есть команда онкоортопедов, собран опыт эндопротезирования при ЗНО костей, хорошо отработаны методики ревизионного эндопротезирования и есть специальное инновационное оборудование, а также высокотехнологичные хирургические инструменты.
В последние годы все более популярны 3D-принтинговые технологии. Это означает, что на основе данных, полученных от лучевой диагностики, выполняется 3D-моделирование операции и изготовление протеза индивидуально для каждого пациента.
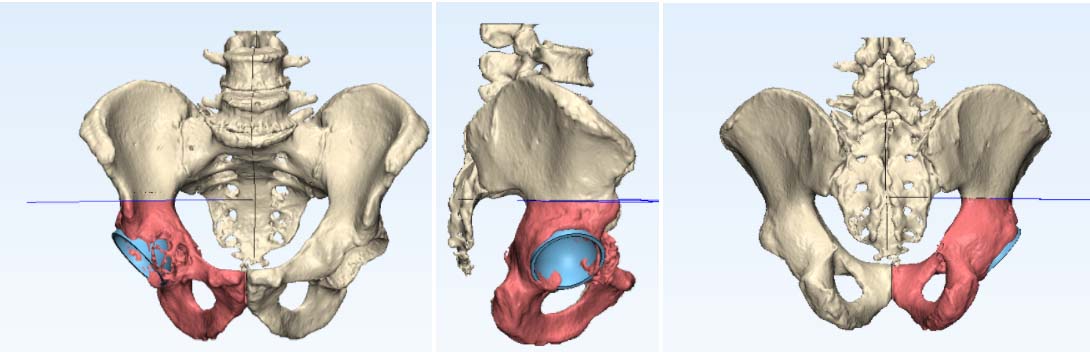
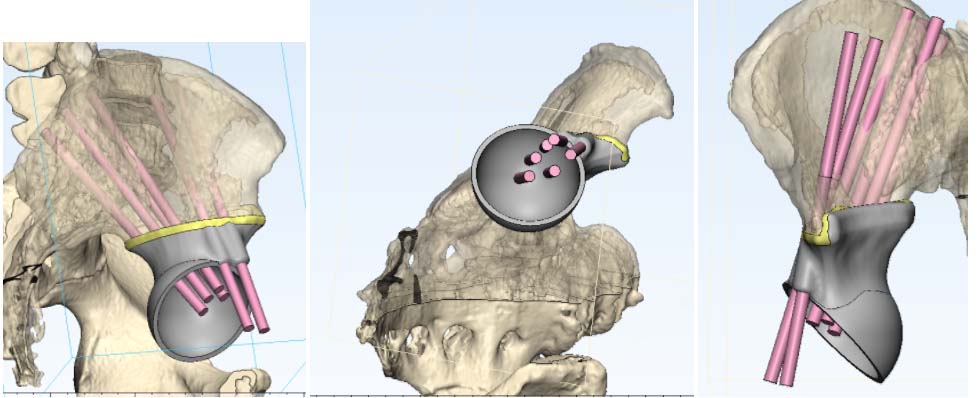
Фото: 3D-моделирование операции
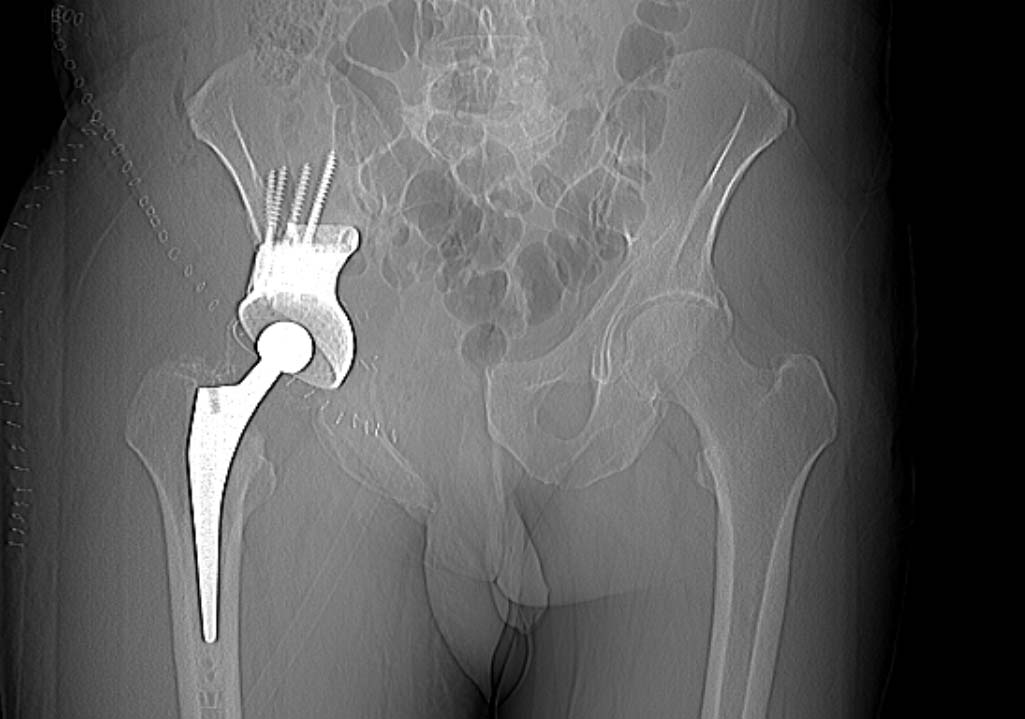
Фото: Эндопротезирование при хондросаркоме тела подвздошной кости
Химиотерапия после операции определяется тем, насколько изменилось заболевание под воздействием лекарств на предоперационном этапе. Если был некроз новообразования 90 %, то после хирургического вмешательства показаны 4 курса химиотерапии теми же цитостатиками. Если степень некроза меньше, то длительность лечения будет примерно 1 год с применением альтернирующих схем, которые включают 5-6 цитостатиков.
Саркомы семейства Юинга – это редкие новообразования, преимущественно молодого возраста. Они имеют повышенную чувствительность к облучению и химиотерапии, требуют комплексного подхода к терапии, которая должна проводиться в специализированных медицинских центрах. В стандартный алгоритм диагностики для первичных новообразований рекомендуется включать сцинтиграфию костей скелета, а также трепан-биопсию костного мозга, потому что наблюдается высокая частота появления метастазов в костях и костном мозге.
После тщательного обследования и биопсии проводится 4-6 циклов индукционной химиотерапии на протяжении 12-24 недель. После этого применяется локальная методика лечения – облучение или радикальная операция, – а далее назначается 6-10 циклов химиотерапии с интервалом в 3 недели. Продолжительность лечения – 1 год.
Радикальное хирургическое вмешательство, если его можно провести, – это лучшая возможность локального контроля.
Лучевая терапия назначается при невозможности проведения радикальной операции, а также обсуждается, если при гистологическом исследовании удаленного материала выявляется недостаточный ответ на лечение, то есть обнаруживается свыше 10 % жизнеспособных клеток опухоли.
Нерадикальное хирургическое вмешательство с последующим облучением эффективно настолько же, насколько просто лучевая терапия. Она проводится в дозах 40-45 Гр при наличии микроскопических остаточных новообразований и 50-60 Гр, если присутствуют макроскопические изменения.
Важный этап лечения больных с первичными опухолями костей – реабилитация. Она позволяет повысить качество жизни как после органосохраняющих, так и после калечащих хирургических вмешательств, ускоряет социализацию пациента.
Тем, кто закончил этап комбинированной терапии, рекомендуется наблюдаться в динамике каждые 3 месяца в первые 2 года, а потом раз в 6 месяцев до 5 лет. Обязательные процедуры – это УЗИ зоны послеоперационного рубца и КТ грудной клетки. Цель данного наблюдения – раннее обнаружение рецидива и ранее начало химиотерапии и хирургического лечения тех метастазов, которые можно резецировать, и рецидивных опухолей, а также предупреждение ортопедических осложнений и выявление нестабильности эндопротеза тоже на ранних сроках.
Дополнительно больным с остеосаркомой рекомендована рентгенография области костного поражения.
Пациентам с саркомой Юинга рекомендуется дополнительно делать УЗИ брюшной полости и периферических лимфоузлов.
Что вам необходимо сделать
Если вы хотите узнать побольше о бесплатных возможностях ФБГУ НМИЦ онкологии им. Н.Н. Петрова Минздрава России, получить очную или заочную консультацию по диагностике и лечению, записаться на приём, ознакомьтесь с информацией на официальном сайте.
Если вы хотите общаться с нами через социальные сети, обратите внимание на аккаунты в ВКонтакте и Одноклассники.
Если вам понравилась статья:
- оставьте комментарий ниже;
- поделитесь в социальных сетях через удобные кнопки: